
【题目】以粉煤灰(主要成分为Al2O3和SiO2,还含有少量的FeO、Fe2O3等)为原料制备Al2O3的流程如下:

(1)“酸浸”时需加入过量的稀硫酸,目的是提高浸取率和________;滤渣的主要成分是__________。
(2)“氧化”过程中,加入H2O2发生反应的离子方程式为____________。
(3)“提纯”过程中,当加入NaOH溶液达到沉淀量最大时,溶液中c(SO42-)∶c(Na+)=_________。
(4)已知Ksp[Fe(OH)3]=1×10-39。“提纯”过程中,当c(Fe3+)<10-6 mol ·L-1时,溶液中c(OH-)>________mol ·L-1。
(5)“沉淀”过程中,通入过量CO2时发生反应的化学方程式为_____________。
【答案】(1)抑制Al3+水解(或为后续反应提供H+),SiO2;
(2)2Fe2++ H2O2+ 2H+=2Fe3++ 2H2O;(3)1∶2;
(4)1×10—11;(5)NaAlO2+ CO2+ 2H2O=Al(OH)3↓+NaHCO3。
【解析】(1)铝离子能够水解,因此“酸浸”时加入过量的稀硫酸,除了可以提高浸取率,还可以抑制Al3+水解;Al2O3和SiO2、FeO、Fe2O3中只有SiO2不能被硫酸溶解,因此滤渣是,故答案为:抑制Al3+水解;SiO2;
(2)“氧化”过程中,加入H2O2能够将亚铁离子氧化,反应的离子方程式为2Fe2+ + H2O2 + 2H+=2Fe3+ + 2H2O,故答案为:2Fe2+ + H2O2 + 2H+=2Fe3+ + 2H2O;
(3)“提纯”过程中,当加入NaOH溶液,生成氢氧化铁和氢氧化铝沉淀,且沉淀完全时,沉淀量达到最大,此时溶液中的溶质为硫酸钠,c(SO42-)∶c(Na+)=1:2,故答案为:1:2;
(4)根据Ksp[Fe(OH)3]=1×10-39。“提纯”过程中,当c(Fe3+)<10-6 mol ·L-1时,溶液中c(OH-)>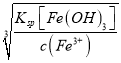 =
=![]() =1×10—11mol ·L-1,故答案为:1×10—11;
=1×10—11mol ·L-1,故答案为:1×10—11;
(5)“沉淀”过程中,通入过量CO2,与溶液中的偏铝酸钠反应生成氢氧化铝沉淀和碳酸氢钠,反应的化学方程式为NaAlO2+ CO2 + 2H2O=Al(OH)3↓+NaHCO3,故答案为:NaAlO2+ CO2 + 2H2O=Al(OH)3↓+NaHCO3。


科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是( )
A.硫化氢气体通入硫酸铜溶液中:S2-+Cu2+=CuS↓
B.4mol/L的NaAlO2溶液和7mol/L的HCl等体积互相均匀混合:4AlO2-+7H++H2O=3Al(OH)3↓+Al3+
C.Ba(OH)2溶液中加入少量的NaHSO4溶液:Ba2++2OH- +2H++SO42-=BaSO4↓+2H2O
D.NaHCO3的水解:HCO3-+H2O![]() CO32-+H3O+
CO32-+H3O+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明Cl2的某些性质。甲同学设计了如图所示的实验装置(部分支撑用的铁架台省略)。

按要求回答下列问题。
(1)若用含有0.2 mol HCl的浓盐酸与足量的MnO2反应制取Cl2,制得的Cl2体积总是小于1.12 L(标准状况)的原因是______________。
(2)①装置B中盛放的试剂名称为________,作用是__________,现象是____________________。
②装置D和E中出现的不同现象说明的问题是_________________。
③装置F的作用是_______________________。
④写出装置G中发生反应的离子方程式______________。
(3)乙同学认为甲同学设计的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液中的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在________与________之间(填装置字母序号),装置中应放入________(填试剂或用品名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na+的浓度不是1 mol/L的溶液是
A. 0.5mol/L的NaCl B. 0.5 mol/L的Na2SO4
C. 1mol/L的NaOH D. 0.5 mol/L的Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“黄金搭档”维生素片中含Ca、Fe、Zn、Cu等元素,其中属于组成生物体的大量元素的是 ( )
A. Ca B. Fe C. Zn D. Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:C(s)+O2(g)=CO2(g) ΔH1
CO2(g)+C(s)=2CO(g) ΔH2
2CO(g)+O2(g)=2CO2(g) ΔH3
4Fe(s)+3O2(g)=2Fe2O3(s) ΔH4
3CO(g)+Fe2O3(s)=3CO2(g)+2Fe(s) ΔH5
下列关于上述反应焓变的判断正确的是
A.ΔH1>0,ΔH3<0 B.ΔH2>0,ΔH4>0
C.ΔH1=ΔH2+ΔH3 D.ΔH3=ΔH4+ΔH5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
①在热化学方程式中无论是反应物还是生成物都必须标明状态 ②所有的化学反应都伴随着能量变化 ③放热反应发生时不必加热 ④吸热反应在加热后才能发生 ⑤化学反应的热效应数值只与参加反应的物质的多少有关 ⑥一般来说,吸热反应在一定条件下也能发生 ⑦依据盖斯定律,反应焓变的大小与反应的途径有关
A.②③⑥⑦ B.③④⑤⑦ C.④⑤⑦ D.③④⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关Ba(OH)2溶液与H2SO4溶液反应的离子方程式中,书写正确的是( )
A.Ba(OH)2+2H++SO42﹣═BaSO4↓+2H2O
B.Ba2++2OH﹣+2H++SO42﹣═BaSO4↓+2H2O
C.Ba2++OH﹣+H++SO42﹣═BaSO4↓+H2O
D.OH﹣+H+═H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com