
| 名称 | 分子式 | 外观 | 沸点 |
| 高氯酸 | HClO4 | 无色液体 | 130℃ |

分析 NaClO3和浓H2SO4在反应器I中反应:3NaClO3+3H2SO4=HClO4+2ClO2↑+3NaHSO4+H2O;生成HClO4、ClO2和NaHSO4,ClO2在反应器II中与二氧化硫、氢氧化钠反应2ClO2+SO2+4NaOH═2NaClO2+Na2SO4+2H2O;生成亚氯酸钠,再得到其晶体;反应器I中得到的溶液通过冷却过滤得到NaHSO4晶体,滤液为HClO4,蒸馏得到纯净的HClO4.
(1)根据上述分析,操作①为过滤分离晶体和溶液;
(2)加入过量的硫酸是为了制得高氯酸,如果硫酸加少了会生成高氯酸钠;
(3)反应器Ⅱ中ClO2与二氧化硫、氢氧化钠反应生成亚氯酸钠;
(4)水的沸点是100℃,HClO4的沸点是130℃,最先蒸馏流出的是水而不是HClO4;
(5)根据方程式3NaClO3+3H2SO4=HClO4+2ClO2↑+3NaHSO4+H2O进行计算;
(6)电解盐酸的电解池中,阳极是Cl-失电子发生氧化反应的过程.
解答 解:NaClO3和浓H2SO4在反应器I中反应生成HClO4、ClO2和NaHSO4,其反应的化学方程式为:3NaClO3+3H2SO4=HClO4+2ClO2↑+3NaHSO4+H2O;冷却溶液时会降低NaHSO4的溶解度,使NaHSO4结晶析出;高氯酸的沸点低,易挥发,蒸馏可以得到纯净的高氯酸,
(1)根据上述分析,操作①为过滤,
故答案为:过滤;
(2)反应器Ⅰ中投料时如果硫酸加少了会生成高氯酸钠,加入过量的硫酸是为了制得高氯酸,
故答案为:为了产物能得到HClO4而不是NaClO4;
(3)反应器Ⅱ中ClO2与二氧化硫、氢氧化钠反应生成亚氯酸钠,其反应的离子方程式为:4OH-+SO2+2ClO2=2ClO2-+SO42-+2H2O,
故答案为:4OH-+SO2+2ClO2=2ClO2-+SO42-+2H2O;
(4)水沸点是100℃,HClO4的沸点是130℃,最先蒸馏流出的是水而不是HClO4,有液体流出时立即收集得到的是谁,不能得到HClO4纯品,因此不合理,
故答案为:不合理,因为水的沸点是100℃,HClO4的沸点是130℃,所以最先蒸馏流出的是水而不是HClO4;
(5)设需要NaClO3x,根据方程式3NaClO3+3H2SO4=HClO4+2ClO2↑+3NaHSO4+H2O,
3×106.5g 100.5g
x 201kg
x=639kg,
故答案为:639;
(6)铂作阳极、铜作阴极电解盐酸时,阳极是Cl-失电子发生氧化反应的过程,即电极反应式为:4H2O+HCl-8e-=HClO4+8H+,
故答案为:4H2O+HCl-8e-=HClO4+8H+.
点评 本题以亚氯酸钠制备为背景,考查了学生阅读题目获取信息的能力、对氧化还原反应相关知识的运用、有关实验操作和简单实验设计能力,以及在新情境下综合运用知识解决问题的能力,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 金属钠着火,立即用水灭火 | |
| B. | 在气体发生装置上直接点燃甲烷气体时,必须先检验甲烷的纯度 | |
| C. | 酒精灯不慎着火,应立即吹熄 | |
| D. | 眼睛里溅进盐酸,立即用 NaOH 溶液洗涤眼睛 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
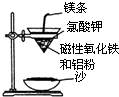 某校高三同学高考前重做以下两个课本实验,请你回答实验过程中的相关问题:
某校高三同学高考前重做以下两个课本实验,请你回答实验过程中的相关问题:| 编号 | 温度/℃ | H2SO4体积/mL | KI溶液体积/mL | H2O体积/mL | 淀粉溶液 /mL | 出现蓝色时间/s |
| A | 39 | 10 | 5 | 5 | 1 | 5 |
| B | TB | 10 | 5 | 5 | 1 | 没出现蓝色 |
| C | 5 | 10 | 5 | 5 | 1 | 39 |
| D | t |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 14.3% | B. | 12.5% | C. | 87.5% | D. | 85.7% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
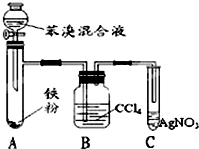 如表是A、B、C三种烃的有关信息;
如表是A、B、C三种烃的有关信息;| A | B | C |
| ①能使溴的四氯化碳溶液褪色; ②比例模型为:  | 1棍模型为: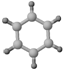 ②平面型结构 | ①能使溴的四氯化碳溶液褪色; ②比例模型为:  ③能与H2在一定条件下反应生成A |
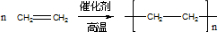 .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素编号 | 元素性质或原子结构 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 第三周期元素的简单离子中半径最小 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
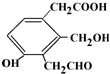 ,等物质的量的该物质,消耗Na、NaOH、NaHCO3的物质的量之比为3:2:1;消耗H2、Br2(水)的物质的量之比为2:1.
,等物质的量的该物质,消耗Na、NaOH、NaHCO3的物质的量之比为3:2:1;消耗H2、Br2(水)的物质的量之比为2:1.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com