
分析 常温下,pH=10的强碱AOH和pH=4的酸H2B等体积混合后溶液显酸性,证明H2B为弱酸,恰好反应生成的是强碱弱酸盐,酸根离子水解溶液成碱性.
解答 解:常温下,pH=10的强碱AOH和pH=4的酸H2B等体积混合后溶液显酸性,证明H2B为弱酸,生成的盐为酸式盐AHB,恰好反应生成的是强碱弱酸盐,生成的盐化学式A2B,酸根离子水解溶液成碱性,离子方程式为B2-+H2O?HB-+OH-;故答案为:AHB;碱; B2-+H2O?HB-+OH-.
故答案为:AHB;碱; B2-+H2O?HB-+OH-.
点评 本题考查了氢离子浓度与氢氧根离子浓度相同的酸碱混合后溶液溶液分析以及盐类水解,题目难度不大.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 日常生活中用无水乙醇杀菌消毒 | |
| B. | 目前加碘食盐中添加的是KIO3 | |
| C. | 绿色食品是不含任何化学物质的食品 | |
| D. | 碘是人体中含量最多的必需微量元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 热激活电池可用作火箭、导弹的工作电源.一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能.该电池总反应为PbSO4+2LiCl+Ca═CaCl2+Li2SO4+Pb.下列有关说法正确的是( )
热激活电池可用作火箭、导弹的工作电源.一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能.该电池总反应为PbSO4+2LiCl+Ca═CaCl2+Li2SO4+Pb.下列有关说法正确的是( )| A. | 常温时,在正负极间接上电流表或检流计,指针不偏转 | |
| B. | 放电过程中,Li+向负极移动 | |
| C. | 每转移0.2mol电子,理论上生成41.4gPb | |
| D. | 正极反应式:Ca+2Cl--2e-═CaCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用水能区分丁醇和苯 | |
| B. | 苯乙烯在合适条件下催化加氢可生成乙基环己烷 | |
| C. | 室温下,在水中的溶解度:丙三醇>苯酚>1-氯丁烷 | |
| D. | 甲苯与氯气在光照下反应主要生成对氯甲苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
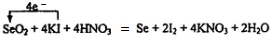 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com