
 反应生成的化合物的结构简式.
反应生成的化合物的结构简式. 科目:高中化学 来源: 题型:选择题
| A. | 100mL | B. | 99mL | C. | 101mL | D. | 98mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HN03溶液混有H2SO4,可加入适量的BaCl2溶液,过滤除去 | |
| B. | 向某溶液中加入稀H2SO4,有无色无味气体生成,说明原溶液中一定含有CO32- | |
| C. | 乙酸乙酯(沸点77℃)中混有乙醇,可以用蒸馏法提纯 | |
| D. | 饱和食盐水可以除去Cl2中的HCl气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+的电子排布图: | |
| B. | HF的电子式: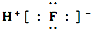 | |
| C. | Fe2+的核外电子排布式:1s22s22p63s23p63d6 | |
| D. | N2的结构简式::N≡N: |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验室用铜制取硫酸铜,将适量硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体.
实验室用铜制取硫酸铜,将适量硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
 ,存在的化学键是离子键、共价键,写出A2B2与水反应的化学方程式2Na2O2+2H2O=4NaOH+O2↑.
,存在的化学键是离子键、共价键,写出A2B2与水反应的化学方程式2Na2O2+2H2O=4NaOH+O2↑.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图的有机物,则该有机物可发生的反应类型有( )
如图的有机物,则该有机物可发生的反应类型有( )| A. | ①②④⑤⑥ | B. | ①②③⑤⑦ | C. | ①②⑤⑥⑦ | D. | ①②④⑤⑦ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com