
���� ��1��ͭ��Ũ������ȷ�Ӧ��������ͭ=���������ˮ��Ũ���ᡢŨ����������ǿ��ʹ�����������γ����������ﱣ��Ĥ��
��2�������������ڴ������������·�����Ӧ����һ��������ˮ��
��3�������������������������ǿ��ǿ�Ӧ�������ᷴӦ�����Ȼ�����ˮ����������������������Һ��Ӧ����ƫ�����ƺ�������
��� �⣺��1��ͭ��Ũ������ȷ�Ӧ��������ͭ=���������ˮ����Ӧ�Ļ�ѧ����ʽΪ��Cu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O��Ũ�����Ũ���Ὣ�������ۻ���������������������ʢװ��
�ʴ�Ϊ��Cu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O��Ũ���ᡢŨ����������ǿ��ʹ�����������γ����������ﱣ��Ĥ�������ۻ���������������������ʢװ��
��2�������������ڴ������������·�����Ӧ����һ��������ˮ����Ӧ�Ļ�ѧ����ʽΪ��4NH3+5O2$\frac{\underline{����}}{��}$4NO+6H2O��
�ʴ�Ϊ��4NH3+5O2$\frac{\underline{����}}{��}$4NO+6H2O��
��3���������������ᷴӦ�����ӷ���ʽΪ��Al��OH��3+3H+=Al3++3H2O������������NaOH��Һ��Ӧ�Ļ�ѧ����ʽΪ��Al��OH��3+NaOH=NaAlO2+2H2O��
�ʴ�Ϊ��Al��OH��3+3H+=Al3++3H2O��Al��OH��3+NaOH=NaAlO2+2H2O��
���� ���⿼�����������ʺ�Ӧ�ã���Ҫ�ǻ�ѧ����ʽ�����ӷ���ʽ����д����Ŀ�ϼ�


 ������������ϵ�д�
������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 84g | B�� | 65.4g | C�� | 67.6g | D�� | 53g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ۺ���ά�صķ���ʽ��Ϊ��C6H10O5��n�����Ե��ۺ���ά�ػ�Ϊͬ���칹�� | |
| B�� | ������ˮ�����������Dz��ų��������ṩ����������� | |
| C�� | ���ࡢ��֬�������ʶ�������Ȼ�߷��ӻ����� | |
| D�� | �ͼ������з�����ζ���ճ������е����ϡ��ǹ��и��ȳ�ʹ�õͼ��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO��ȼ����Ϊ-566 kJ/mol | |
| B�� | �ڢ۷�Ӧʱ�����������������ʹ��H��С | |
| C�� | ��Ͷ��1molCO2��3molH2��һ�������³�ַ�Ӧ����ų�����49 kJ | |
| D�� | ��������ͬ������CO2����ų�������C2H2����CO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������ཫ̫����ת��Ϊ���ܵij��ò��� | |
| B�� | ���ʹ����ƹ��ά�IJ��� | |
| C�� | �ֹ��Ʊ��ߴ��ȵ��ʹ費�漰������ԭ��Ӧ | |
| D�� | ����������ᷴӦ�������������ᷴӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ˮ���뱽�У���ˮ����ɫ��dz�������뱽�����˼ӳɷ�Ӧ | |
| B�� | �������е�̼ԭ��֮��ļ���ȫ��ͬ����һ�ֽ��ڵ�����˫��֮��Ķ��صļ� | |
| C�� | 1 mol����ͱ�ϩ�Ļ�����ȫȼ������3 mol H2O | |
| D�� | һ�������£�Cl2���ڼױ��ı���������Ϸ���ȡ����Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
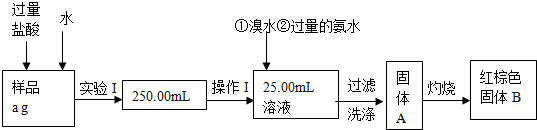

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ϩ�ܿ�������ʳƷ��װ�� | |
| B�� | ��ҵ���õ����ˮ�Ȼ����ķ����Ƶ����� | |
| C�� | ������ϩ���ϵ��ϻ�����Ϊ�����˼ӳɷ�Ӧ | |
| D�� | ���ࡢ��֬�������ʶ��ܷ���ˮ�ⷴӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
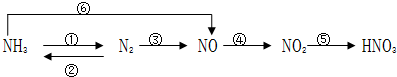
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com