
以下有关原子结构及元素周期律的叙述正确的是
A.第IA族元素铯的两种同位素137Cs比133Cs多4个质子
B.同周期元素(除0族元素外)从左到右,原子半径逐渐减小
C.第 ⅦA元素从上到下,其氢化物的稳定性逐渐增强
D.同主族元素从上到下,单质的熔点逐渐降低
B
【解析】质子数相同而中子数不同的同一元素的不同原子互称为同位素,即137Cs和133Cs的质子数相同,137和133表示二者的质量数,因此A不正确;同周期元素(除0族元素外)从左到右,随着核电荷数的逐渐增多,原子核对外层电子对吸引力逐渐增强,因此原子半径逐渐减小,B正确;同主族元素从上到下,随着核电荷数的逐渐增多,电子层数逐渐增多,原子半径逐渐增大,原子核对外层电子对吸引力逐渐减弱,非金属性逐渐减弱,因此第 ⅦA元素从上到下,其氢化物的稳定性逐渐减弱,C不正确;同主族元素从上到下,单质的熔点有的逐渐降低,例如IA,而有的逐渐升高,例如 ⅦA,所以选项也D不正确。答案选B。


科目:高中化学 来源:2014高考名师推荐化学常见仪器的使用(解析版) 题型:选择题
下列①~④四个图是某学习小组设计的相关物质的制备装置,其中正确的是
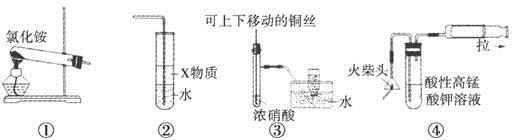
A.用装置①可以制备氨气
B.若装置②中X物质为苯,可用于实验室制备少量氨水,并防止发生倒吸
C.装置③可用于制备并收集少量NO2气体
D.装置④可用火柴头燃烧制备少量SO2,并检验产生的SO2
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学实验专题(解析版) 题型:实验题
S2C12是一种金黄色易挥发的液体,常用作橡胶硫化剂。某化学兴趣小组 拟设计实验制备少量的S2C12,査阅资料知S2Cl2在水中易发生歧化反应(一部分硫元素化 合价升高,另一部分化合价 降低)。加热条件下硫单质和干燥、纯净的Cl2反应即可生成S2C12,反应的化学方程式为:2S+Cl2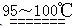 S2Cl2。
S2Cl2。
反应涉及的几种物质的熔沸点如下:
物质 | S | S2Cl2 |
沸点/℃ | 445 | 138 |
熔点/℃ | 113 | -76 |
该小组设计的制备装置如下图(夹持仪器已略去)
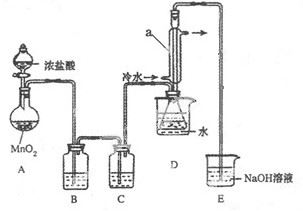
回答下列问题:
(1)连接好实验装置后的第一步实验操作是______。
(2)实验中需要加热的仪器是 (填写字母)
(3)装置B、C中的试剂分别是 。
(4)装置D中仪器a的作用是 。
(5)反应结束后从锥形瓶内混合物中分离出产品的方法是____________。
(6)若实验过程中缺少C装置,发现产品浑浊不清,请用化学方程式表示其原因____________。
(7)实验完毕,小组中的一位同学把剩余浓盐酸倒入E烧杯中,发现有黄绿色剌激性气体产生。用离子方程式表示产生该现象的原因____________。
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学基本营养物质(解析版) 题型:选择题
化学与生产、生活密切相关,下列有关说法正确的是
A.生物柴油是不同酯组成的混合物,可用“地沟油”制得
B.合成纤维、人造纤维及碳纤维都属于有机高分子材料
C.纤维素在人体内可水解为葡萄糖,故可做人类的营养物质
D.聚乙烯塑料制品可用于食品的包装,该塑料的老化是由于发生了加成反应
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学周期表、核素(解析版) 题型:选择题
短周期元素R、T、Q、W在元素周期表中的相对位置如右下图所示,其中T所处的周期序数与族序数相等。下列判断不正确的是
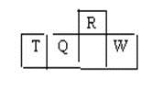
A.最简单气态氢化物的热稳定性:R>Q
B.最高价氧化物对应水化物的酸性:Q<W
C.原子半径:T>Q>R
D.含T的盐溶液一定显酸性
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学可充电池的反应规律(解析版) 题型:选择题
一种太阳能电池的工作原理如下图所示,电解质为铁氰化钾K3[Fe(CN)6]和亚铁氰化钾K4[Fe(CN)6]的混合溶液,下列说法不正确的是
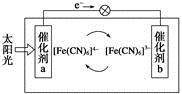
A.K+移向催化剂b
B.催化剂a表面发生的化学反应:[Fe(CN)6]4--e-=[Fe(CN)6]3-
C.Fe(CN)在催化剂b表面被氧化
D.电解池溶液中的[Fe(CN)6]4-和[Fe(CN)6]3-浓度基本保持不变
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学可充电池的反应规律(解析版) 题型:选择题
科学家们在研制一种吸气式的锂—空气电池,工作时吸收空气中的氧气在多孔金制成的正极表面上反应。总反应可表示为2Li+O2 Li2O2,下列有关说法正确的是
Li2O2,下列有关说法正确的是
A.充电时,多孔金制成的电极外接电源负极
B.放电时,吸收空气中22.4 L的O2,就有2 mol e-从电池负极流出
C.放电时,Li+从负极向正极移动
D.该电池可使用含Li+的水溶液作电解质溶液
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学原电池四种型与金属腐蚀、保护(解析版) 题型:选择题
一种新型燃料电池,以镍板为电极插入KOH溶液中,分别向两极通入乙烷(C2H6)和氧气,其中某一电极反应式为C2H6+18OH--14e-=2CO32-+12H2O。有关此电池的推断不正确的是
A.通入氧气的电极为正极
B.参加反应的O2与C2H6的物质的量之比为7∶2
C.放电一段时间后,KOH的物质的量浓度将下降
D.放电一段时间后,正极区附近溶液的pH减小
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学化学平衡常数(解析版) 题型:选择题
将固体NH4I置于密闭容器中,在一定温度下发生下列反应:
①NH4I(s) NH3(g)+HI(g);
NH3(g)+HI(g);
②2HI H2(g)+I2(g)
H2(g)+I2(g)
达到平衡时,c(H2)=0.5mol·L-1,c(HI)=4mol·L-1,则此温度下反应①的平衡常数为
A.9 B.16 C.20 D.25
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com