��������1������ˮ�����ڸ����·�Ӧ����������������������
��2����Һ���к����������ӣ����������£�ClO
3-����Fe
2+ΪFe
3+����������ԭΪCl
-�����ݵ�ʧ������ȡ�����غ㡢�����غ���ƽ��
��3����CΪKKO
3��KOH�Ļ�����Fe
2O
3���ȹ����Ƶø�����أ���ȱ������ΪK
2FeO
4��H
2O�����ݵ�ʧ������ȡ������غ���ƽ��
��4���ٷ�Ӧԭ�����еⵥ�����ɺ����ģ��ⵥ������������ʾ��ɫ����ѡ����Ϊָʾ�������ⵥ����ȫ��Ӧ����Һ����ɫ��Ϊ��ɫ���ݴ��жϵζ��յ㣻
�ڸ��ݷ�Ӧ2Fe
3++2I
-�T2Fe
2++I
2��I
2+2S
2O
32-�T2I
-+S
4O
62-�ҳ���ϵʽFe
3+��S
2O
32-��Ȼ����ݹ�ϵʽ����������ӵ����ʵ������ٸ���c=
�������Ԫ�غ���������˫��ˮ������S
2O
32-�����ʵ�����Ӱ���ж���
��5��������Һ�е�Fe
3+����KSCN��Һ��������Һ�е�Fe
2+�������Ը��������Һ��K
3[Fe��CN��]
6��Һ��
���
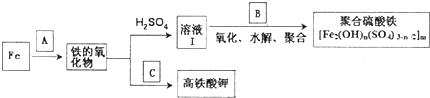
�⣺��1��Fe��ˮ�����ڸ����·�Ӧ�Ļ�ѧ����ʽΪ��3Fe+4H
2O��g��
Fe
30
4+4H
2��
�ʴ�Ϊ��3Fe+4H
2O��g��
Fe
30
4+4H
2��
��2�������������̿�֪�����������������ᷴӦ��������������������������Һ���к����������ӣ����������£�ClO
3-����Fe
2+ΪFe
3+����������ԭΪCl
-�����ݻ��ϼ����������ƽ����ƽ������ӷ���ʽΪ��6Fe
2++ClO
3-+6H
+�T6Fe
3++Cl
-+3H
2O��
�ʴ�Ϊ��6Fe
2++ClO
3-+6H
+�T6Fe
3++Cl
-+3H
2O��
��3��KNO
3��KOH�Ļ���д������Fe
2O
3���ȹ����Ƶ�K
2FeO
4����ȱ������һ��ΪK
2FeO
4��K
2FeO
4����Ԫ�ػ��ϼ�Ϊ+6�����������Ӵ�+3�۱�Ϊ+6�ۣ����ϼ�����3�ۣ����ϼ���������3��2=6�ۣ�KNO
3��NԪ�ش�+5��ΪKNO
2�е�+3�ۣ����ϼ۽���2�ۣ��ϼ���С������Ϊ6��������������ϵ��Ϊ1��KNO
3��ϵ��Ϊ3��Ȼ����������غ㶨����ƽ����ƽ��ķ���ʽΪ��Fe
2O
3+3KNO
3+2KOH=K
2FeO
4+3KNO
2+H
2O��
�ʴ�Ϊ��1��3��4��2��K
2FeO
4��3��2��H
2O��
��4����Fe
3+����I
-����I
2���������������ѡ�������Һ��ָʾ�������������һ�������������Һʱ����ɫ��ʧ���Ұ���Ӳ���ɫ˵�����յ㣬
�ʴ�Ϊ�����ۣ���Һ����ɫ����ɫ�ұ��ְ���Ӳ���ɫ��
����2Fe
3++2I
-�T2Fe
2++I
2��I
2+2S
2O
32-�T2I
-+S
4O
62-�ɵã�Fe
3+��S
2O
32-����n��Fe
3+��=n��S
2O
32-��=0.1000mol/L��0.02L=0.002mol����Ԫ���ܺ���Ϊ��
=5.6g/L��
H
2O
2Ҳ������I
-����I
2����������������û�г����������������������Һ���ƫ��������ƫ�ߣ�
�ʴ�Ϊ��5.6��ƫ�ߣ�
��5��������ҺI�е�Fe
2+��Fe
3+�ķ���Ϊ��ȡ��Һ���������Թ��У����������ữ���ټ�����������Һ����Һ��ɫ������ɫ��ɻ�ɫ���dz������Fe
2+����ȡ��Һ���������Թ��У��������軯����Һ������ɫ�������ɣ�����Fe
2+������ȡ��Һ���������Թ��У��μ����軯����Һ�������Ϊ��ɫ��֤������������
�ʴ�Ϊ��ȡ��Һ���������Թ��У����������ữ���ټ�����������Һ����Һ��ɫ������ɫ��ɻ�ɫ���dz������Fe
2+����ȡ��Һ���������Թ��У��������軯����Һ������ɫ�������ɣ�����Fe
2+������ȡ��Һ���������Թ��У��μ����軯����Һ�������Ϊ��ɫ��֤�����������ӣ�




 ij��ɫ���������O2��CO��CO2��HCl��NH3��NO��Br2�е�һ�ֻ�����ɣ�ͨ��ͼ��ϴ��ƿ������������٣���װ��ǰ�������ֱ����������ͨ������ܣ���ʢ��Na2O2��������ʺ���ɫ���������ƶ���ȷ���ǣ�������
ij��ɫ���������O2��CO��CO2��HCl��NH3��NO��Br2�е�һ�ֻ�����ɣ�ͨ��ͼ��ϴ��ƿ������������٣���װ��ǰ�������ֱ����������ͨ������ܣ���ʢ��Na2O2��������ʺ���ɫ���������ƶ���ȷ���ǣ������� ijͬѧ�������ͼװ�ã��г�����ʡ�ԣ�����ϵ��ʵ��ʱ����ҩƷA��μ��뵽����B�У����������ʵ��ش����⣮
ijͬѧ�������ͼװ�ã��г�����ʡ�ԣ�����ϵ��ʵ��ʱ����ҩƷA��μ��뵽����B�У����������ʵ��ش����⣮ ��ͼ��ʾ����ƿ��ʢ������X���ι���ʢ��Һ��Y������ѹ�ιܽ�ͷ��ʹҺ��Y����ƿ�У���һ����ɼ�С����a��������X��Һ��Y�������ǣ�������
��ͼ��ʾ����ƿ��ʢ������X���ι���ʢ��Һ��Y������ѹ�ιܽ�ͷ��ʹҺ��Y����ƿ�У���һ����ɼ�С����a��������X��Һ��Y�������ǣ������� ���а�ˮ�����ᡢ���ᡢ�Ȼ��������Һ����ش��������⣺
���а�ˮ�����ᡢ���ᡢ�Ȼ��������Һ����ش��������⣺ ��˫ϩ�ϳɣ�Ҳ�ɱ�ʾΪ
��˫ϩ�ϳɣ�Ҳ�ɱ�ʾΪ ��
��


