
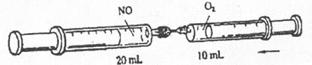
| A.气体变为红棕色 |
| B.气体体积仍为20mL |
| C.气体变为混合物 |
| D.气体中氮原子与氧原子物质的量之比等于l:2 |
科目:高中化学 来源:不详 题型:填空题
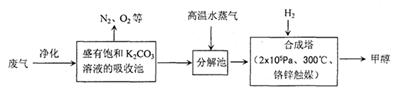
 虑温度对反应速率的影响外,还主要考虑了 。
虑温度对反应速率的影响外,还主要考虑了 。| A.过滤 | B.分液 | C.蒸馏 | D.结晶 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
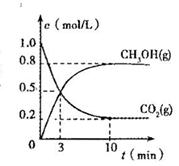
 CH3OH(g) △H < 0
CH3OH(g) △H < 0| A.v正(H2)=2 v正(CH3OH) | B.v正(H2)=v正(CO) |
| C.容器内压强保持不变 | D.混合气体的密度不变 |
 浓度为0.6mol/L,试求该温度下的化学平衡常数。
浓度为0.6mol/L,试求该温度下的化学平衡常数。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2AB(g)达到平衡状态的标志是( )
2AB(g)达到平衡状态的标志是( )| A.容器内总的压强不随时间变化 |
| B.容器内的总物质的量不随时间变化 |
| C.单位时间内生成2n mol AB的同时生成n mol B2 |
| D.容器内A2、B2、AB的物质的量之比是1∶1∶2时的状态 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2C(g)△H<0,为了使平衡向生成
2C(g)△H<0,为了使平衡向生成 C的方向移动,应选择的条件是〔 〕
C的方向移动,应选择的条件是〔 〕查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.只要是有气体参加或生成的化学反应,化学平衡都会受压强的影响 |
| B.化学平衡向正反应方向移动,反应物的转化率不一定增大 |
| C.增大反应物的浓度可以使反应物活化分子百分数增多,从而加快化学反应速率 |
D.化学平  衡发生移动,则化学平衡常数一定也发生相应的变化 衡发生移动,则化学平衡常数一定也发生相应的变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
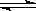 O2(g)+ 2NO(g) ΔH>0,达到
O2(g)+ 2NO(g) ΔH>0,达到 平衡。当改变其中一个条件X,Y随X的变化符合图中曲线的是
平衡。当改变其中一个条件X,Y随X的变化符合图中曲线的是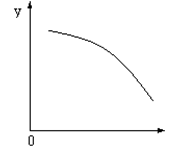
| A.当X表示温度时,Y表示NO的物质的量 |
| B.当X表示压强时,Y表示NO2的转化率 |
| C.当X表示反应时间时,Y表示混合气体的密度 |
| D.当X表示NO2的物质的量时,Y表示O2的物质的量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2SO3(g) , 如果2min内SO2的浓度由6 mol/L下降为2 mol/L,用O2浓度变化来表示的反应速率为 __________________。
2SO3(g) , 如果2min内SO2的浓度由6 mol/L下降为2 mol/L,用O2浓度变化来表示的反应速率为 __________________。
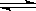 2SO3 △H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a~b过程中改变的条件可能是___________________; 请将增大压
2SO3 △H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a~b过程中改变的条件可能是___________________; 请将增大压 强时的反应速率变化情况画在c~d处:
强时的反应速率变化情况画在c~d处:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com