


科目:高中化学 来源: 题型:阅读理解
| 实验步骤 | 预期现象和结论 |
| 步骤1:将菠菜研磨后,浸泡、过滤得到澄清待测溶液. | |
| 步骤2:调节溶液至弱碱性,滴加足量CaCl2溶液. | 出现白色沉淀,说明菠菜中可能含有草酸盐和碳酸盐. |
| 步骤3:取步骤2的沉淀于试管中, 加入足量1 mol?L-1 HCl,将产生的气体通入足量澄清石灰水中. 加入足量1 mol?L-1 HCl,将产生的气体通入足量澄清石灰水中. |
沉淀溶解,澄清石灰水变浑浊,说明菠菜中含有碳酸盐. 沉淀溶解,澄清石灰水变浑浊,说明菠菜中含有碳酸盐. |
| 步骤4: 向步骤3得到的溶液中滴加几滴0.01 mol?L-1 KMnO4. 向步骤3得到的溶液中滴加几滴0.01 mol?L-1 KMnO4. |
溶液紫红色褪去,说明菠菜中含有草酸盐. 溶液紫红色褪去,说明菠菜中含有草酸盐. |
| 0.0100mol/L×V×10-3L×5×100mL×88g/mol |
| 2×25mL×mg |
| 0.0100mol/L×V×10-3L×5×100mL×88g/mol |
| 2×25mL×mg |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
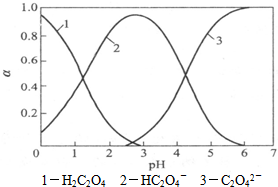 草酸(H2C2O4)是一种二元弱酸,受热能分解,它在水溶液中存在形式的分布与pH关系如图所示:
草酸(H2C2O4)是一种二元弱酸,受热能分解,它在水溶液中存在形式的分布与pH关系如图所示:
| ||
| ||
| 酸 | 铁锈[Fe(OH)3]溶解量/g | 水垢(CaCO3)溶解量/g |
| 盐酸 | 0.7911 | 全溶 |
| 磷酸 | 0.1586 | 微溶 |
| 草酸 | 0.7399 | 0.0036 |
| 醋酸 | 0.1788 | 0.1655 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度 | v(H2C2O4) | v(KMnO4) | KMnO4褪色时间 |
| 40℃ | 10ml | 10ml | 40s |
| 40℃ | 20ml | 20ml |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com