
【题目】已知A、B、C、D是中学化学中常见的四种不同粒子,它们之间存在如下图所示的转化关系:

(1)如果A、B、C、D均是10电子的粒子,请写出:
A的电子式_____________;D的电子式____________;
(2)如果A和C是18电子的粒子,B和D是10电子的粒子,请写出:
①A与B在溶液中反应的离子方程式:____________________________________
②根据上述离子方程式,可判断C与B结合质子的能力大小是(用化学式或离子符号表示)________>________。
【答案】
![]() HS-+OH-=S2-+H2O OH- S2-
HS-+OH-=S2-+H2O OH- S2-
【解析】
(1)10电子粒子,原子有Ne(也可看做分子);离子有Na+、Mg2+、Al3+、N3-、O2-、F-、OH-、NH4+、H3O+,分子有CH4、NH3、H2O、HF;
根据图示的转化关系可知,C+H+→A,B+H+→D,A+B→C+D,根据以上的粒子,可推测出A、B、C、D分别为NH4+、OH-、NH3、H2O,据此解题;
(2) 18电子微粒有:Ar、K+、Ca2+、Cl-、S2-、H2O2、F2、HCl、HS-、H2S、PH3、SiH4等。
(1)由分析可知,A的电子式为 ;D的电子式为
;D的电子式为![]() ;
;
(2)如果A和C是18电子的粒子,B和D是10电子的粒子,可推测出A、B、C、D分别为HS-、OH-、S2-、H2O。
①A与B在溶液中反应的离子方程式为:HS-+OH-=S2-+H2O;
②弱酸根对应的酸,若酸性越弱,则其与H+结合的能力越强。根据上述离子方程式,可判断酸性HS->H2O ,所以结合质子的能力大小是S2-<OH-。


科目:高中化学 来源: 题型:
【题目】钛被誉为第三金属,广泛用于航天航空等领域。硼化钒(VB2)-空气电池的放电反应为4VB2+11O2===4B2O3+2V2O5,以该电池为电源制备钛的装置如图所示。
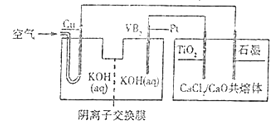
下列说法正确的是( )
A. 电解过程中,OH-由阴离子交换膜右侧向左侧迁移
B. Pt极反应式为2VB2+22OH--22e-===V2O5+2B2O3+11H2O
C. 电解过程中,铜极附近电解质溶液的pH减小
D. 若石墨极只收集到4.48LCl2气体,则理论上制备4.8gTi
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将少量CuSO4粉末溶于盛有水的试管中得到一种天蓝色溶液,先向试管里的溶液中滴加氨水,首先形成蓝色沉淀。继续滴加氨水,沉淀溶解,得到深蓝色的透明溶液;若加入乙醇溶剂,将析出深蓝色的晶体。
(1)溶液中呈天蓝色微粒的结构可用示意图表示为_______,1 mol该天蓝色微粒所含的σ键数目为________。
(2)加入乙醇的作用是__________。
(3)写出蓝色沉淀溶解成深蓝色溶液的离子方程式______________。
(4)得到的深蓝色晶体是[Cu(NH3)4]SO4·H2O,晶体中Cu2+与NH3之间的化学键称为_____,提供空轨道的微粒是_______,提供孤电子对的成键原子是_____,该晶体中配体分子的VSEPR模型为_______。
(5)下列说法正确的是_________
a.[Cu(NH3)4]SO4组成元素中电负性最大的是氮元素
b.氨气分子和水分子的空间构型不同,氨气分子的键角大于水分子的键角
c.氨气极易溶于水,是因为氨气分子和水分子之间形成2种不同的氢键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关 2个电化学装置的叙述正确的是 ( )

A.图I,由于盐桥中的![]() 移向
移向![]() 溶液,一段时间后,使溶液中的正电荷数量增加
溶液,一段时间后,使溶液中的正电荷数量增加
B.图I,在不改变总反应的前提下,可用![]() 替换
替换![]() ,用石墨替换 Cu棒
,用石墨替换 Cu棒
C.图II,通电后![]() 和
和![]() 先从阳极区移动到阴极,然后阴极才发生反应
先从阳极区移动到阴极,然后阴极才发生反应![]()
D.图II,通电后,由于 ![]() 向阳极迁移,导致阳极附近 pH升高
向阳极迁移,导致阳极附近 pH升高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在水溶液中1 mol ClOx-(x=0,1,2,3,4)的能量(kJ)相对大小如图所示,下列有关说法正确的是( )
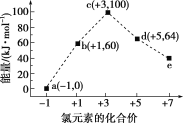
A.e是ClO3-
B.b→a+c反应的活化能为60 kJ·mol-1
C.a、b、c、d、e中c最稳定
D.b→a+d反应的热化学方程式为3ClO-(aq)=2Cl-(aq)+ClO3-(aq) ΔH=-116 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年IUPAC命名117号元素为TS(中文名“![]() ” tián),Ts的原子核外最外层电子数是7,下列说法不正确的是
” tián),Ts的原子核外最外层电子数是7,下列说法不正确的是
A.TS是第七周期第VIIA族元素B.中子数为176的Ts核素符号是![]() Ts
Ts
C.Ts在同周期元素中金属性最弱D.Ts的同位素原子具有相同的电子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以氨气代替氢气来研发氨燃料电池是当前科研的一个热点,氨燃料电池使用的电解质溶液是KOH溶液,电池反应为4NH3+3O2![]() 2N2+6H2O。下列有关说法错误的是( )
2N2+6H2O。下列有关说法错误的是( )
A. 燃料电池的能量转化率一般比普通的电池高
B. 氨燃料电池在放电时,负极反应为2NH3-6e-+6OH-===N2+6H2O
C. 以氨气代替氢气的主要原因是氨气易液化、易储存
D. 氨燃料电池在充电时,在阴极N2得电子被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】S16O2与18O2在高温条件下发生反应2SO2+O2![]() 2SO3,达到化学平衡后,平衡混合物中含18O的微粒( )
2SO3,达到化学平衡后,平衡混合物中含18O的微粒( )
A. 只有SO3 B. 只有SO2、SO3 C. 有SO2、SO3、O2 D. 只有O2、SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知硅及其化合物之间存在如图转化关系。其中A是制造芯片和光电池的主要原料;B是含硅化合物中的一种气体;某些C可作干燥剂或催化剂的载体;D是一种黏合剂,能将磨砂玻璃黏合在一起,E是一种比H2CO3酸性还弱的酸。
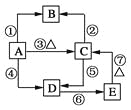
试回答下列问题:
(1)写出A、C、E的化学式:A________、C________、E________。
(2)①~⑦反应中,属于氧化还原反应的是________,属于置换反应的是______,属于离子反应的是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com