
| A������þʧ�����ö�����̼��������𣻽�����ʧ��Ҳ�����ö�����̼��� |
| B������Ag2O���Եõ�������������CuOҲ����ȡ����ͭ |
| C����ҵ���õ������MgCl2�ķ�����ȡ����þ����Ҳ���õ������AlCl3�ķ�����ȡ������ |
| D��Al��Sֱ�ӻ��Ͽ��Եõ�Al2S3��Fe��Sֱ�ӻ���Ҳ�ɵõ�Fe2S3 |
| ||


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CH3Cl |
| B��CH3CH2-C��CH3��2CH2Br |
| C��CH3CH2-C��CH3��2Cl |
| D��CH2Br-CH��CH3��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��c��H+��=
| ||
| B����������Һ�У�HCO3-��Na+��K+��CH3COO- | ||
| C������ϡ���ᷴӦ��ȡH2�����Һ�У�K+��AlO2-��SO42-��Br- | ||
| D�����ʵĿ�����SO2��NO��N2��NH3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A������2SO2��g��+O2��g��?2SO3��g������H=-QkJ/mol����Q��0������Ӧ�г���1mol SO2��������������Ӧʱ���ų�������һ����
| ||
| B���Ȼ�ѧ����ʽ�еĻ�ѧ��������ʾ���ʵ����������Ƿ��� | ||
| C�����ʱ���Ƽ������������жƲ���������ӵ���Һ�����Һ | ||
| D��1 mol H2SO4��1 molBa��OH��2��Ӧ����BaSO4����ʱ�ų����Ƚ����к��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��2L 0.5mol/L NaCl��Һ |
| B��3L 0.3mol/L Na2SO4��Һ |
| C��1L 0.4mol/L Na2CO3��Һ |
| D��4L 0.15mol/L Na3PO4��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| CCl4 |
| NBS |
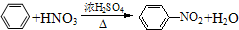
| ŨH2SO4 |
| 170�� |
| A���ڢ� | B���ۢ� | C���٢� | D���ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������ӵ������������Ħ������������ |
| B�������ӵ������������Ħ����������� |
| C����������ܶȡ������Ħ������ |
| D�������ӵ��������������Ħ���������ܶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��3��3-�������� |
| B��2��3-����-2-�һ����� |
| C��2-�һ����� |
| D��2��5��5-�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��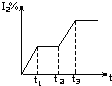 |
B�� |
C��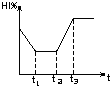 |
D��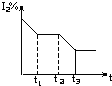 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com