
| A. | 核外电子排布完全相同的两种微粒,其化学性质一定相同 | |
| B. | 凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布 | |
| C. | 核外电子排布相同的两中性原子一定属于同种元素 | |
| D. | 阴离子的核外电子排布一定与上一周期稀有气体元素原子的核外电子排布相同 |
分析 A.核外电子排布完全相同的两种微粒,其化学性质不一定相同,如K+与S2-等;
B.一些过渡元素形成的离子不一定具有稀有气体的核外电子排布;
C.核外电子排布相同的两中性原子,质子数一定相等,一定属于同种元素;
C.阴离子的核外电子排布与同周期稀有气体元素原子的核外电子排布相同.
解答 解:A、K+与S2-、Kr的核外电子排布完全相同,但化学性质不同,故A错误;
B.一些过渡元素形成的离子不一定具有稀有气体的核外电子排布,如Fe3+的核外电子排布式为1s22s22p63s23p63d5,故B错误;
C.两种中性原子核外电子排布相同,核外电子数相同,质子数相同,为同一元素的不同核素,二者核外同位素,故C正确;
D.主族元素形成的简单阳离子与上一周期稀有气体元素原子的核外电子排布相同,阴离子的核外电子排布与同周期稀有气体元素原子的核外电子排布相同,故D错误.
故选:C.
点评 本题考查核外电子排布,难度不大,注意采取列举反例法,列举法是选择中经常使用的方法.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:高中化学 来源: 题型:选择题
| A. | 钠溶于水的反应:2Na+2H2O═2NaOH+H2↑ | |
| B. | 碳酸钠溶液和稀醋酸反应:CO2-3+2H+═H2O+CO2↑ | |
| C. | 向Ba(OH)2溶液中逐滴加入硫酸氢钠溶液至中性:2H++SO2-4+Ba2++2OH-═BaSO4↓+2H2O | |
| D. | 硫化亚铁中加入稀硝酸:FeS+2H+═Fe2++H2S↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 金属钛性能优越,被誉为继Fe、Al后应用广泛的“第三金属”.
金属钛性能优越,被誉为继Fe、Al后应用广泛的“第三金属”.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲酸 | B. | 乙二酸 | C. | 丙酸 | D. | 丁酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 热稳定性:Y的气态氢化物>Z的气态氢化物 | |
| B. | Z的最高价氧化物对应水化物的分子式为H2ZO4 | |
| C. | X元素的单质能与所有强酸发生反应放出H2 | |
| D. | R的核外电子数与OH-的核外电子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含4molSi-O键的二氧化硅晶体中氧原子数为2NA | |
| B. | 标准状况下,含3NA个σ键的甲醛分子所占的体积约为22.4L | |
| C. | 2molNO和1molO2混合,在密闭容器中充分反应,容器内的分子数小于2NA | |
| D. | 1molFe与一定量的硝酸反应,转移的电子数为0.2NA~0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
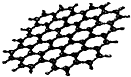 最近,科学家从石墨中分离出来的石墨烯是已知最薄、最坚硬的物质.可以制成纳米材料.其结构如图所示:下列关于石墨烯的说法正确的是( )
最近,科学家从石墨中分离出来的石墨烯是已知最薄、最坚硬的物质.可以制成纳米材料.其结构如图所示:下列关于石墨烯的说法正确的是( )| A. | 属于高分子化合物 | B. | 与金刚石互为同分异构体 | ||
| C. | 性质稳定不能与氧气等物质反应 | D. | 能导电 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | VB2电极发生的电极反应为:2VB2+11H2O-22e-═V2O5+2B2O3+22H+ | |
| B. | 外电路中电子由c电极流向VB2电极 | |
| C. | 电解过程中,c电极表面先有红色物质析出,后有气泡产生 | |
| D. | 若B装置内的液体体积为100 mL,则CuSO4溶液的物质的量浓度为0.05 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用10mL量筒量取8.10mL稀盐酸 | |
| B. | 用pH计测得某溶液的pH为2.3 | |
| C. | 用pH试纸测定溶液的pH时,需先用蒸馏水润湿试纸 | |
| D. | 可用50.00mL碱式滴定管量取20.00mL KMnO4溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com