
分析 (1)根据配制一定物质的量浓度的溶液配制步骤来解答;
(2)盐酸应用酸式滴定管量取,然后调节液面;
(3)待测液为NaOH,选择碱式滴定管或移液管;强酸与强碱反应,可用酚酞作指示剂,滴定前,酚酞遇碱变红,滴定后若变无色,停止滴定;
(4)由c(酸)V(酸)=c(碱)V(碱)计算c(NaOH),进一步计算500mL溶液中NaOH的物质的量,利用样品的质量5.0g计算质量分数;
(5)根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$,判断不当操作对V(标准)影响,从而判断对浓度的影响.
A.转移待测液至容量瓶时,未洗涤烧杯,NaOH的物质的量减少;
B.酸式滴定管用蒸馏水洗涤后,直接装盐酸,盐酸的浓度偏低,消耗酸偏大;
C.滴定时,反应容器摇动太激烈,有少量液体溅出,NaOH的物质的量减少;
D.滴定到终点时,滴定管尖嘴悬有液滴,消耗盐酸偏大;
E.读酸式滴定管开始时仰视,读数偏大,而读终点时俯视,读数偏小,二者之差偏小.
解答 解:(1)操作步骤有计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解(可用量筒量取水加入烧杯),并用玻璃棒搅拌,加速溶解,冷却后转移到500mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀,所以以上操作中出现的五处错误:①未冷却就转移;②烧杯、玻璃棒未洗涤;③未用玻璃棒引流;④未用胶头滴管滴加至刻度线;⑤未振荡、摇匀;
故答案为:未冷却就转移;烧杯、玻璃棒未洗涤;未用玻璃棒引流;未用胶头滴管滴加至刻度线;未振荡、摇匀;
(2)盐酸应用酸式滴定管量取,调节液面位置在0刻度或0刻度下某一刻度;
故答案为:酸式;0刻度或0刻度下某一刻度;
(3)待测液为NaOH,选择碱式滴定管,放在锥形瓶中;强酸与强碱反应,可用酚酞作指示剂,滴定前,酚酞遇碱变红,到达滴定终点时观察到溶液颜色由浅红色变为无色;
故答案为:碱式滴定管;酚酞;红色;无;
(4)c(HCl)=0.2mol/L,V(HCl)=20.00mL,V(NaOH)=20.00mL,由c(酸)V(酸)=c(碱)V(碱)可知c(NaOH)=0.2mol/L,则500mL溶液中NaOH的物质的量为:0.5L×0.2mol/L=0.1mol,则NaOH的质量为0.1mol×40g/mol=4.0g,所以5.0g样品中NaOH的质量分数为$\frac{4.0g}{5.0g}$×100%=80.0%,
故答案为:80.0%;
(5)A.转移待测液至容量瓶时,未洗涤烧杯,NaOH的物质的量减少,造成V(标准)偏小,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析,结果偏小,故A正确;
B.酸式滴定管用蒸馏水洗涤后,直接装盐酸,盐酸的浓度偏低,造成V(标准)偏大,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析,结果偏大,故B错误;
C.滴定时,反应容器摇动太激烈,有少量液体溅出,NaOH的物质的量减少,造成V(标准)偏小,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析,结果偏小,故C正确;
D.滴定到终点时,滴定管尖嘴悬有液滴,造成V(标准)偏大,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析,结果偏大,故D错误;
E.读酸式滴定管开始时仰视,读数偏大,而读终点时俯视,读数偏小,二者之差偏小,造成V(标准)偏小,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析,结果偏小,故E正确;
故答案为:ACE.
点评 本题考查中和滴定操作,题目难度中等,注意把握实验基本方法,能会分析导致误差的不当操作,注意把握实验操作要点和注意事项.


 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
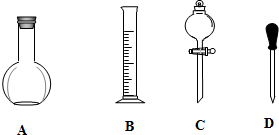 实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.
实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
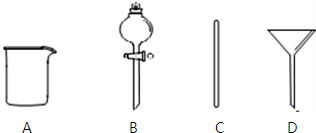 实验室需要0.1mol•L-1NaOH溶液480mL.
实验室需要0.1mol•L-1NaOH溶液480mL.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 时间/m i n | 0 | 1 | 2 | 3 | 4 | 5 |
| n(SO2)/mol | 0.2 | 0.16 | 0.13 | 0.11 | 0.08 | 0.08 |
| A. | 当容器中气体的密度不变时,该反应达到平衡状态 | |
| B. | 用SO3表示0~4 min内该反应的平均速率为0.01 mol/(L•m i n) | |
| C. | 升高温度时,逆反应速率大于正反应速率,平衡常数K值会减小 | |
| D. | 平衡时再通入18O2,平衡右移,达新平衡时,18O仅存在于O2和SO3中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应中氧化剂和还原剂的质量比为1:2 | |
| B. | 反应中生成了8g Cu2S | |
| C. | 反应中有0.2×6.02×1023个电子转移 | |
| D. | 反应中有1.6g硫被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,11.2 LCO2所含的原子数为1.5NA | |
| B. | 标准状况下,22.4 L CCl4中所含分子数为NA | |
| C. | 标准状况下,18g水所含原子数为NA | |
| D. | 常温常压下,48 g O2与O3混合物含有的氧原子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙元素的族序数比甲元素的族序数大 | |
| B. | 甲、丙元素最高价氧化物对应水化物的酸性强弱顺序为:甲<丙 | |
| C. | 原子半径由大到小的顺序为:丙>甲>乙 | |
| D. | 含乙元素的化合物数目比含甲或丙元素的化合物数目多 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com