
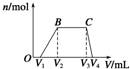
 1L某混合溶液,可能含有的离子如下表:
1L某混合溶液,可能含有的离子如下表:| 可能大量含有的阳离子 | H+、K+、Mg2+、Al3+、NH
| ||||
| 可能大量含有的阴离子 | Cl-、Br-、I-、CO
|
2- 3 |
- 2 |
+ 4 |
2- 3 |
- 2 |
2- 3 |
- 2 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、10gH2和10gO2 |
| B、5.6LN2和11gCO2 |
| C、9g H2O和0.5mol Cl2 |
| D、标准状况下224mlH2和0.1mol N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、28Si、29Si、30Si 是不同元素的三种原子 |
| B、28Si、29Si、30Si 互称为同位素 |
| C、28Si、29Si、30Si 分别含有14、15、16个质子 |
| D、28Si、29Si、30Si都含有14个中子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
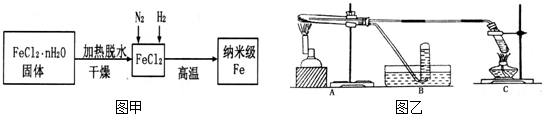
| 实验步骤 | 实验操作 | 实验现象 |
| ① | 将反应后得到的黑色粉末(假定均匀)取出少量放入另一试管中,加入少量盐酸,微热 | 黑色粉末逐渐溶解,溶液呈浅绿色,有少量气泡产生 |
| ② | 向上述溶液中滴加几滴KSCN溶液,震荡 | 溶液没有出现红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
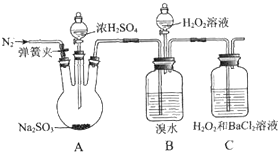 为探究H2O2、SO2、Br2氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验).
为探究H2O2、SO2、Br2氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验).| 实验操作 | 实验现象 |
| ⅰ.打开A中分液漏斗活塞,滴加浓硫酸 | A中有气泡产生,B中红棕色溴水褪色,C中有白色沉淀 |
| ⅱ.取C中沉淀加入盐酸 | C中白色沉淀不溶解 |
| ⅲ.打开B中分流漏斗活塞,逐滴滴加H2O2 | 开始时颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、11.2 g |
| B、2.8 g |
| C、5.6 g |
| D、无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=1的溶液中:Na+、Mg2+、SO42-、HCO3- |
| B、含有大量Fe3+的溶液中:Al3+、Cu2+、SO42-、Cl- |
| C、加入A1能放出H2的溶液中:K+、NH4+、NO3-、Cl- |
| D、能使甲基橙呈红色的溶液中:Na+、AlO2-、NO3-、HCO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com