
【题目】碳酸钠是一种重要的化工原料,主要采用氨碱法生产。回答下列问题:
(1)碳酸钠俗称 , 可作为碱使用的原因是(用离子方程式表示)。
(2)已知:①2NaOH(s)+CO2(g) ![]() Na2CO3(s)+H2O(g) ΔH1=127.4 kJ·mol1 ②NaOH(s)+CO2(g)
Na2CO3(s)+H2O(g) ΔH1=127.4 kJ·mol1 ②NaOH(s)+CO2(g) ![]() NaHCO3(s) ΔH1=131.5 kJ·mol1
NaHCO3(s) ΔH1=131.5 kJ·mol1
反应2Na2CO3(s) ![]() Na2CO3(s)+ H2O(g) +CO2(g)的ΔH= kJ·mol1 , 该反应的平衡常数表达式K=。
Na2CO3(s)+ H2O(g) +CO2(g)的ΔH= kJ·mol1 , 该反应的平衡常数表达式K=。
(3)向含有BaSO4固体的溶液中滴加Na2CO3溶液,当有BaCO3沉淀生成时溶液中 ![]() =。已知Ksp(BaCO3)=2.6×109 , Ksp(BaSO4)=1.1×1010。
=。已知Ksp(BaCO3)=2.6×109 , Ksp(BaSO4)=1.1×1010。
【答案】
(1)纯碱;CO32﹣+H2O?HCO3﹣+OH﹣
(2)+135.6;c(H2O)?c(CO2)
(3)![]()
【解析】解:(1)碳酸钠俗称纯碱;Na2CO3为强碱弱酸盐,CO32﹣离子水解方程式为CO32﹣+H2OHCO3﹣+OH﹣ , 使溶液呈碱性, 所以答案是:纯碱;CO32﹣+H2OHCO3﹣+OH﹣;(2)①2NaOH(s)+CO2(g)═Na2CO3(s)+H2O(g)△H1=﹣127.4kJmol﹣1
②NaOH(s)+CO2(g)═NaHCO3(s)△H1=﹣131.5kJmol﹣1
, ①﹣2×②得,2NaHCO3(s)═Na2CO3(s)+H2O(g)+CO2(g)△H=+135.6kJmol﹣1;K=c(H2O)c(CO2),
所以答案是:+135.6;c(H2O)c(CO2);(3)Ksp(Ba SO4)=c(Ba2+)(SO42﹣)=1.1×10﹣10;Ksp(BaCO3)=c(Ba2+)c(CO32﹣)=2.6×10﹣9 ,
所以 ![]() =
= ![]() =
= ![]() =
= ![]() ,
,
所以答案是: ![]() .
.
【考点精析】解答此题的关键在于理解反应热和焓变的相关知识,掌握在化学反应中放出或吸收的热量,通常叫反应热.


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
【题目】在一定温度下,某容积固定的密闭容器中,建立下列化学平衡:C(s)+H2O(g)![]() CO(g)
CO(g)
+H2(g)。下列叙述中不能说明上述可逆反应已达到化学平衡状态的是( )
A. 体系的压强不再发生变化
B. v正(CO)=v逆(H2O)
C. 生成n mol CO的同时生成n mol H2
D. 1 mol H—H键断裂的同时断裂2 mol H—O键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向容积为2 L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如下图所示,对该反应的推断合理的是( )
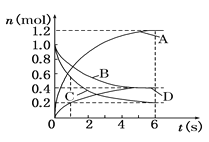
A. 该反应的化学方程式为3B+4D![]() 6A+2C
6A+2C
B. 反应进行到1 s时,v(A)=v(D)
C. 反应进行到6 s时,B的平均反应速率为0.05 mol/(L·s)
D. 反应进行到6 s时,各物质的反应速率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 三聚氰酸(C3H3N3O3)的结构式为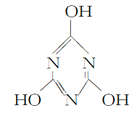 ,它属于共价化合物
,它属于共价化合物
B. 只含H、N、O三种元素的化合物,可能是离子化合物,也可能是共价化合物
C. NaHCO3、CH3COONa均含有离子键和共价键
D. 化合物MgO、H2O中化学键的类型相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g)+O2(g)2SO3(g)是制备硫酸的重要反应.下列叙述正确的是( )
A.催化剂V2O3不改变该反应的逆反应速率
B.增大反应体系的压强,反应速率一定增大
C.该反应是放热反应,降低温度将缩短反应达到平衡的时间
D.在t1、t2时刻,SO3(g)的浓度分别是c1、c2 , 则时间间隔t1~t2内,SO3(g)生成的平均速率为v= ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】证明氨水是弱碱的事实是
A.氨水与硫酸发生中和反应B.氨水能使紫色石蕊试液变蓝
C.0.1 mol/L的NH4Cl溶液的pH值为5.1D.浓氨水易挥发
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二硫化碳(CS2,标况下为液体)能够在氧气中完全燃烧生成CO2和SO2,今用0.228g CS2在448mL O2(在标准状况下)中完全燃烧,反应后气体混合物在标准状况下的体积是( )
A. 112mL B. 224mL C. 336mL D. 448mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外实验小组设计的下列实验不合理的是( )
A. 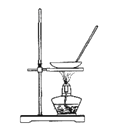 蒸干NH4Cl饱和溶液制备NH4Cl晶体
蒸干NH4Cl饱和溶液制备NH4Cl晶体
B. 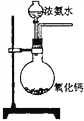 实验室制备少量氨气
实验室制备少量氨气
C. 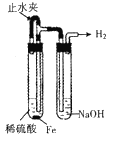 制备并观察氢氧化亚铁
制备并观察氢氧化亚铁
D. 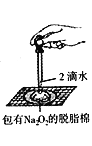 证明过氧化钠与水反应放热
证明过氧化钠与水反应放热
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com