
 向含有1mol HNO3和1mol H2SO4的混合溶液中逐渐加入铁粉至过量,溶液中金属阳离子a、b与所加铁粉的物质的量的关系如图所示(已知稀硝酸的还原产物只有NO).下列有关判断不正确的是( )
向含有1mol HNO3和1mol H2SO4的混合溶液中逐渐加入铁粉至过量,溶液中金属阳离子a、b与所加铁粉的物质的量的关系如图所示(已知稀硝酸的还原产物只有NO).下列有关判断不正确的是( )| A、a表示Fe3+的关系曲线 |
| B、n1=0.75 |
| C、p点时,n(Fe2+)=0.5625 mol |
| D、向p点溶液中加入铜粉,最多可溶解14.4g |
 解:A、向含有1molHNO3和1molH2SO4的混合溶液中逐渐加入铁粉至过量,现实发生反应:Fe+4H++NO3-═Fe3++NO↑(气体)+2H2O,铁过量后是2Fe3++Fe=3Fe2+,a是表示Fe3+的关系曲线,故A正确;
解:A、向含有1molHNO3和1molH2SO4的混合溶液中逐渐加入铁粉至过量,现实发生反应:Fe+4H++NO3-═Fe3++NO↑(气体)+2H2O,铁过量后是2Fe3++Fe=3Fe2+,a是表示Fe3+的关系曲线,故A正确;| 3 |
| 4 |
| 2 |
| 0.45 |
| 64 |
| Y |


 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:高中化学 来源: 题型:
| A、只有①②④ | B、只有②③ |
| C、①③④ | D、①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、B>Cu>A |
| B、A>Cu>B |
| C、B>A>Cu |
| D、A>B>Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、5.6 g Fe与100 mL1.5 mol/LHNO3反应转移的电子数为0.2NA |
| B、1 molHCl气体中的粒子数与0.5 mo1/L盐酸中溶质粒子数相等 |
| C、在标准状况下,22.4 LCH4与18 gH2O含有的质子数均为10 NA |
| D、CO和N2为等电子体,22.4 L的CO气体与l mol N2所含的电子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SO2、H2、O2 |
| B、SO2、H2S、H2 |
| C、NO、NO2、O2 |
| D、NH3、N2、HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.6 mol SO2+0.3 mol O2+0.4 mol SO3 |
| B、4.0 mol SO2+2.0 mol O2 |
| C、2.0 mol SO2+1.0 mol O2+2.0 mol SO3 |
| D、3.0 mol SO2+0.5 mol O2+1.0 mol SO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
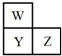 W、X、Y、Z四种短周期元素.已知X原子的核外电子数和Ne原子相差1,在同周期中X原子半径最大,W、Y、Z在周期表中的相对位置如图,Z的非金属性在同周期元素中最强.下列说法不正确的是( )
W、X、Y、Z四种短周期元素.已知X原子的核外电子数和Ne原子相差1,在同周期中X原子半径最大,W、Y、Z在周期表中的相对位置如图,Z的非金属性在同周期元素中最强.下列说法不正确的是( )| A、简单离子半径:Y>X |
| B、最高价氧化物对应水化物的酸性:Z>Y |
| C、W与X形成的化合物属于离子化合物 |
| D、W、X、Z只能形成一种化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②③④ | B、①②④ |
| C、③④ | D、①②③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com