
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2012-2013学年辽宁省本溪一中高二第二次月考化学试卷(带解析) 题型:填空题
(16分)图中X、Y、Z为单质,其他为化学物,它们之间存在如下转化关系(部分产物已略去)。其中,A俗称磁性氧化铁;E是不溶于水的酸性氧化物,能与氢氟酸反应。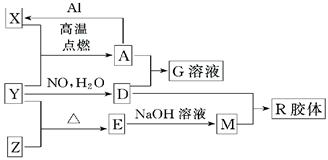
回答下列问题:
⑴组成单质Y的元素在周期表中的位置是 ;M中存在的化学键类型 为 ;R的化学式是 。
⑵一定条件下,Z与H2反应生成ZH4,ZH4的电子式为 。
⑶已知A与1molAl反应转化为X时(所有物质均为固体)。放出a KJ热量。写出该反应的热化学方程式: 。
⑷写出A和D的稀溶液反应生成G的离子方程式: 若转移0.6mol电子,生成的气体在标况下体积为
⑸向含4mol D的稀溶液中,逐渐加入X粉末至过量。假设生成的气体只有一种,请在坐标系中画出n(X2+)随n(X)变化的示意图,并标出n(X2+)的最大值。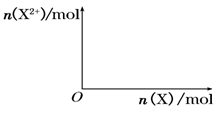
查看答案和解析>>
科目:高中化学 来源:2014届辽宁省高二第二次月考化学试卷(解析版) 题型:填空题
(16分)图中X、Y、Z为单质,其他为化学物,它们之间存在如下转化关系(部分产物已略去)。其中,A俗称磁性氧化铁;E是不溶于水的酸性氧化物,能与氢氟酸反应。
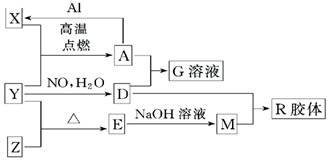
回答下列问题:
⑴组成单质Y的元素在周期表中的位置是 ;M中存在的化学键类型 为 ;R的化学式是 。
⑵一定条件下,Z与H2反应生成ZH4,ZH4的电子式为 。
⑶已知A与1molAl反应转化为X时(所有物质均为固体)。放出a KJ热量。写出该反应的热化学方程式: 。
⑷写出A和D的稀溶液反应生成G的离子方程式: 若转移0.6mol电子,生成的气体在标况下体积为
⑸向含4mol D的稀溶液中,逐渐加入X粉末至过量。假设生成的气体只有一种,请在坐标系中画出n(X2+)随n(X)变化的示意图,并标出n(X2+)的最大值。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com