
����ѧ����ѡ��2����ѧ�뼼����(15��)����ˮ������Ũ��ˮ��Դ������������ۺ����ú�ˮ����Ҫ;��֮һ��һ�����Ƚ���ˮ������õ�ˮ���ٴ�ʣ���Ũ��ˮ��ͨ��һϵ�й���������ȡ������Ʒ��
�ش��������⣺
��1�����иĽ����Ż���ˮ�ۺ����ù��յ�������������е���________(�����)��
���û�������ȡ��ˮ ����߲��ֲ�Ʒ������
���Ż���ȡ��Ʒ��Ʒ�� �ܸĽ��ء��塢þ�ȵ���ȡ����
��2�����á���������������Ũ��ˮ����Br2�����ô������ա����绯ΪBr����BrO3-��û�в���CO2��Ӧ�����ӷ�Ӧ����ʽΪ ��
��3����ˮ��þ��һ�ι�����������ͼ��
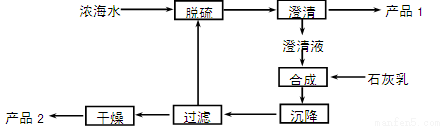
Ũ��ˮ����Ҫ�ɷ����£�
���� | Na�� | Mg2�� | Cl�� | SO42�� |
Ũ��/(g��L��1) | 63.7 | 28.8 | 144.6 | 46.4 |
�ù��չ����У��������Ҫ��Ӧ��������_______����ò�Ʒ2�����ӷ�Ӧ����ʽΪ ��Ũ��ˮ��������Ϊ90������1 LŨ��ˮ���ɵõ���Ʒ2������Ϊ________g��
��4����MgCl2��6H2O�Ʊ�MgCl2ʱ��������HCl�������Χ�м��ȡ���Ŀ���� ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ��ԭ�и�һ��ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
������ͼ��ʾת����ϵ��X����±�أ���˵������ȷ����

A��2H(g) +2X(g) == 2HX(g) ��H3��0
B��;��������HX�ķ�Ӧ����;���أ����Ԧ�H1 = ��H2 + ��H3
C��Cl��Br��I�ķǽ��������μ���������;�������յ�������������
D��;��������HCl�ų�������������HBr�Ķ࣬˵��HCl��HBr�ȶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�Ϻ��з����������ڶ�ѧ�ڵ��в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���Ӿ硶��ɫ���㡷�����dz��չʾ�ˡ��㡱���������ͼ���������Ǿ��з�����ζ��Һ�壬����˵���У�����������ij�ֻ�ѧ���ʵ���
A���þƾ�������ȡijЩ�����е������㾫���Ƴ���ˮ
B������ʱ��һЩ�Ͼƺ�ʳ�ף�ʹ�˸���
C������ˮϴ�����ȥ�������ˮЧ����
D������ˮ���в�ͬ����ζ������Ϊ���в�ͬ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡ�ʳ��и�����ģ���ۻ�ѧ�Ծ��������棩 ���ͣ�ʵ����
��18�֣����ᣨH2C2O4����һ�ְ�ɫ���壬�۵���101�桫102�棬��Լ��157��ʱ��ʼ������189.5��ֽ⣬�dz��õĹ�ҵԭ�ϡ����ò���ͺ������ϣ�������þ�Ͻ�Ϊ������ȡ����������֪����ĸơ�þ������������ˮ��
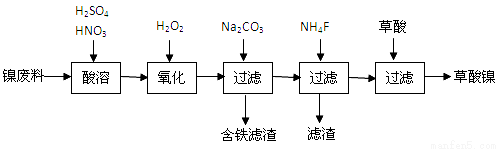
��1�����������ж�ν��й��ˡ�ʵ���ҽ��й��˲������õ�����̨���ձ���������������Ҫ ��
��2��������������������̼������Һ��pH��4.0 ~ 4.5���ң�����̼������Һ�������� ��
�ټ���NH4F��Ŀ���� ��
��3������ͼ��ʾ����������ɵ�װ����̽���������ȷֽ�IJ��

��ʵ���У��۲쵽��ˮ����ͭ������ϴ��ƿ���ڳ���ʯ��ˮ����ǣ��ڸ���ܼ��촦��ȼ�ݳ������壬�ձ��ڱڸ��еij���ʯ��ˮ����ǣ�֤����������______________��Eװ�������Ķ�Ҳ��֤����������������֤��������______________________________��
��װ�õ�����˳��Ϊ__________________��Cװ�õ�������____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡ�ʳ��и�����ģ���ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
���¹����л����������ʶ��ȷ����
A��ij����CnH2n��2��һ�������У����й��ۼ�����Ŀ��3n��1
B����HNO3�ữ��AgNO3��Һ����CCl4���Ƿ�����Ԫ��
C�����ȵ�ͭ˿���Ժ��Ҵ������û���Ӧ��������
D��ʯ�ͻ����õ��IJ�Ʒ��ΪҺ�壬ú�����õ��IJ�Ʒ��Һ��Ҳ�й���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ��Ҵ�и���4����Ͽ������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��10.7 g Mg��Al��Fe��ɵĺϽ���������������������Һ�У�������״����3.36 L���塣��ȡ�������ĺϽ����ڹ��������У����ɱ�״����7.84 L���壬��Ӧ�����Һ�м������NaOH��Һ���õ��������ʵ���Ϊ
A��0.1 mol B��0.2 mol C��0.25 mol D��0.3 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ��ƶ���
��10�֣���֪����R��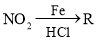 ��
��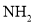
�ڱ�����ԭ�е�ȡ�������µ����ȡ�������뱽����λ��������Ӱ�졣
�������ñ���ԭ���Ʊ�һϵ�л������ת����ϵͼ��
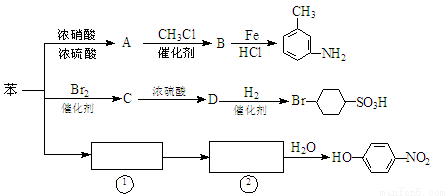
��1��Aת��ΪB�Ļ�ѧ����ʽ��_______________________________________��
��2��ͼ�С������١��ڡ�ʡ���˷�Ӧ��������д���١������ʵĽṹ��ʽ��
��________________________����____________________________��
��3��B�ڱ����ϵĶ��ȴ����� ��ͬ���칹�塣
��4���л��� ������ԭ�� ����ǡ����ǡ�����ͬһƽ���ϡ�
������ԭ�� ����ǡ����ǡ�����ͬһƽ���ϡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
������Һ���������ʵ���Ũ�ȹ�ϵ��ȷ����
A��25��ʱ��pH=7��NH4Cl��NH3��H2O�����Һ��c(H+)= c(OH��)= c(NH4+)=c(Cl��)
B��25��ʱ��pH=2��HCOOH��pH=12��NaOH�������ϣ�c (HCOO��)+ c(H+)>c(Na+)+c(OH��)
C��0.1mol/LNa2S��Һ��c(OH��)=c(H+)+c(HS��)+c(H2S)
D��0.1mol/LNa2CO3��Һ��0.1mol/L NaHCO3��Һ�����c(CO32-)+2c(HCO3-)+2c(H2CO3)=3c(Na+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�Ĵ�ʡ�����и߶���ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���������ֳư�������أ��ŵ�ʱ���ܷ�ӦΪ��Fe��Ni2O3��3H2O===Fe(OH)2��2Ni(OH)2�������йظõ�ص�˵������ȷ����
A����صĵ��ҺΪ������Һ������ΪNi2O3������ΪFe
B����طŵ�ʱ��������ӦΪFe��2OH����2e��=Fe(OH)2
C����س������У�����������Һ��pH����
D����س��ʱ��������ӦΪ2Ni(OH)2��2OH����2e��=Ni2O3��3H2O
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com