
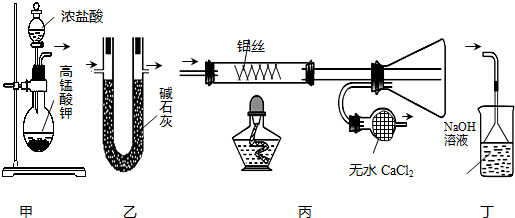
| A. | 用装置甲制取氯气 | B. | 用装置乙干燥氯气 | ||
| C. | 用装置丙制取并收集AlCl3 | D. | 用装置丁处理丙中排出的尾气 |
分析 A.高锰酸钾溶液和浓盐酸反应生成氯气且不需要加热;
B.氯气和碱石灰反应,所以不能用碱石灰干燥氯气;
C.加热条件下氯气和Al反应生成氯化铝,氯化铝易水解,无水氯化钙能吸收水分且和氯化铝不反应;
D.氯气有毒,不能直接排空,但氯气能和NaOH溶液反应生成易溶于水的物质.
解答 解:A.高锰酸钾溶液和浓盐酸反应生成氯气且不需要加热,应该采用固液混合不加热型装置,故A正确;
B.氯气和碱石灰反应,所以不能用碱石灰干燥氯气,应该用浓硫酸干燥氯气,故B错误;
C.加热条件下氯气和Al反应生成氯化铝,氯化铝易水解,无水氯化钙能吸收水分且和氯化铝不反应,所以能实现实验目的,故C正确;
D.氯气有毒,不能直接排空,但氯气能和NaOH溶液反应生成易溶于水的物质NaCl、NaClO,所以能实现实验目的,故D正确;
故选B.
点评 本题考查化学实验方案评价,为高频考点,涉及物质制备、仪器选取、气体干燥、尾气处理等基本操作,明确实验原理及基本操作方法、物质性质是解本题关键,注意C中氯化铝的性质,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 滴有碘水的淀粉溶液10ml分成两等份于两支试管,分别加入稀硫酸和唾液1ml,振荡,前者褪色快 | |
| B. | 恒温下,将盛有NO2和N2O4的平衡体系加压,体系颜色最终变浅 | |
| C. | 草酸溶液与酸性KMnO4溶液混合后,由于生成物对反应有催化作用,会使反应速率加快 | |
| D. | 在K2Cr2O7溶液中滴加浓硫酸,溶液颜色由橙色变黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
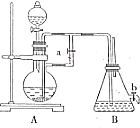 如图所示装置,可用来制取和观察Fe(OH)2在空气中被氧化的须色变化.实验时必须使用铁屑和6mol/L的硫酸,其他试剂任选.
如图所示装置,可用来制取和观察Fe(OH)2在空气中被氧化的须色变化.实验时必须使用铁屑和6mol/L的硫酸,其他试剂任选.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3+HCl═NH4Cl | B. | 4NH3+5O2 $\frac{\underline{\;\;△\;\;}}{\;}$ 4NO+6H2O | ||
| C. | 3CuO+2NH3 $\frac{\underline{\;\;△\;\;}}{\;}$ 3Cu+N2+3H2O | D. | 8NH3+3Cl2 $\frac{\underline{\;\;△\;\;}}{\;}$ 6NH4Cl+N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com