
| A. | H2XO2-在溶液中既可发生电离,又可发生水解 | |
| B. | c(H2XO2-)+c(HXO22-)+c(XO23-)+c(H3XO2)=0.01mol•L-1 | |
| C. | c(H+)=c(OH-)+c(H3XO2) | |
| D. | c(Na+)+c(H+)=c(OH-)+c(H2XO2-) |
分析 某弱酸H3XO2只有一种钠盐:NaH2XO2,说明H3XO2为一元酸,NaH2XO2溶液中只存在H3XO2、H2XO2-,结合电荷守恒、物料守恒解答该题.
解答 解:A.H3XO2为一元酸,H2XO2-在溶液中不能发生电离,故A错误;
B.溶液中不存在HXO22-、XO23-,故B错误;
C.由电荷守恒可知c(Na+)+c(H+)=c(OH-)+c(H2XO2-),由物料守恒可知c(Na+)=c(H3XO2)+c(H2XO2-),二者联式可得c(OH-)=c(H+)+c(H3XO2),故C错误;
D.c(Na+)+c(H+)=c(OH-)+c(H2XO2-)为溶液的电荷守恒式,故D正确.
故选D.
点评 本题考查离子浓度大小比较,为高频考点,侧重考查学生分析判断能力,明确H3XO2为一元酸是解本题关键,很多同学往往认为该三元酸是弱酸而导致错误,为易错题.


 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案科目:高中化学 来源: 题型:选择题
| A. | Na+、Cu2+、Cl-、SO42- | B. | AlO2-、K+、CO32-、Na+ | ||
| C. | Cl-、Al3+、NH4+、HCO3- | D. | Na+、Ca2+、Cl-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
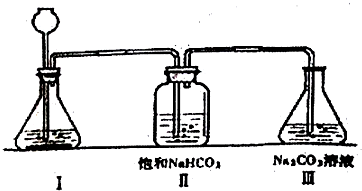
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
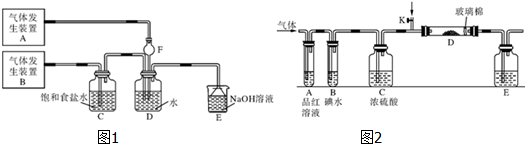
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.65ab | B. | 14.2g | C. | 14.2bg | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该反应热化学方程式为X(g)+3Y(g)?2Z(g),△H=-(E2-E1) | |
| B. | 若图Ⅲ中甲表示压强,乙表示Z的含量,其变化符合图Ⅲ中的曲线 | |
| C. | 若容器容积为10L,t1=10s,则前10s内的平均反应速率为v(Y)=0.006mol•L-1s-1 | |
| D. | 若该体系在373K下反应,则达到平衡所需时间小于t1,且达到平衡时c(X)>0.3mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧两种元素只能组成H2O | |
| B. | 导热性等属于水的化学性质 | |
| C. | 0℃时冰的密度比液态水的密度小 | |
| D. | 液态水两种形态间转化需断裂O-H键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 取该溶液1 mL稀释至100 mL后,pH约等于3 | |
| B. | 向该溶液中加入pH为13的氢氧化钡溶液恰好完全中和 | |
| C. | 该溶液中硝酸电离出的c(H+)与水电离出的c(H+)之比值为10-12 | |
| D. | 该溶液中水电离出的c(H+)是pH为3的硝酸中水电离出的c(H+)的100倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴苯中的苯(NaOH溶液,分液) | |
| B. | 乙醇中的水(新制的氧化钙,蒸馏) | |
| C. | 乙酸中的乙醇(金属钠,蒸馏) | |
| D. | 苯中的甲苯(酸性高锰酸钾溶液,分液) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com