
现代建筑的门窗框架常用电解加工成的古铜色硬铝制造,取硬铝样品进行如下实验(每一步中的试剂均过量):
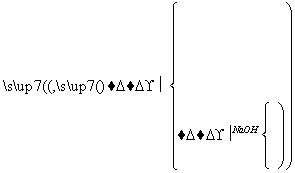
由此可推知,硬铝的组成为( )
A.Al、Cu、Mg、Si、Mn B.Al、Mg、Si、Zn
C.Al、Fe、C、Si D.Al、Si、Zn、Na
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
美国圣路易斯大学研制了一种新型的乙醇电池,用质子(H+)溶剂,在200oC左右时供电。电池总反应为:C2H5OH +3O2=2CO2 +3H2O,电池示意如下图,下列说法正确的是
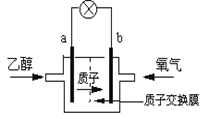
A.a极为电池的正极
B.电池工作时电子由b极沿导线经灯泡再到a极
C.电池正极的电极反应为:4H+ + O2 + 4e=2H2O
D.电池工作时,1mol乙醇被氧化时就有6mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上以黄铜矿(主要成分CuFeS2)为原料制备金属铜,有如下两种工艺。
I.火法熔炼工艺:将处理过的黄铜矿加入石英,再通入空气进行焙烧,即可制得粗铜。
(1)焙烧的总反应式可表示为:2CuFeS2 + 2SiO2+5O2=2Cu+2FeSiO3+4SO2,该反应的氧化剂是 。
(2)焙烧过程产生的SO2会造成污染,下列处理SO2的方法,不合理的是 。
A.高空排放 B.用纯碱溶液吸收制备亚硫酸钠
C.用氨水吸收后,再经氧化制备硫酸铵 D.用BaCl2溶液吸收制备BaSO3
(3)炉渣主要成分有FeO、Fe2O3、SiO2、Al2O3等,为得到Fe2O3,加盐酸溶解后,后续处理过程中,未涉及到的操作有 。
A.过滤 B.加过量NaOH溶液 C.蒸发结晶 D.灼烧 E.加氧化剂
II.FeCl3溶液浸取工艺:其生产流程如下图所示
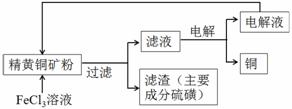
(4)浸出过程中,CuFeS2与FeCl3溶液反应的离子方程式为 。
(5)该工艺流程中,可以循环利用的物质是 (填化学式)。
(6)若用石墨电极电解滤液,写出阳极的电极总反应式 。
(7)黄铜矿中含少量Pb,调节C1- 浓度可控制滤液中Pb2+的浓度,当c(C1-)=2mo1·L-1时溶液中Pb2+物质的量浓度为 mol·L-1。[已知KSP(PbCl2)=1 x 10-5]
查看答案和解析>>
科目:高中化学 来源: 题型:
取两份铝片,第一份与足量盐酸反应,第二份与足量烧碱溶液反应,同温同压下放出相同体积的气体,则消耗的HCl和NaOH的物质的量之比为( )
A.1∶1 B.2∶1
C.3∶1 D.1∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列变化不可通过一步实验直接完成的是( )
A.Al(OH)3―→Al2O3
B.Al2O3―→Al(OH)3
C.Al―→[Al(OH)4]-
D.Al3+―→Al(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
CuS和Cu2S都能溶于硝酸,它们高温灼烧的产物相同,以下鉴别CuS和Cu2S两种黑色粉末的方法合理的是( )
A.将两种样品分别溶于硝酸,区别所产生的气体
B.将两种样品分别溶于硝酸,区别溶液的颜色
C.取两种同质量的样品分别加高温灼烧,区别残留固体的质量
D.取两种同质量的样品分别加高温灼烧,区别残留固体的颜色
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)写出离子反应方程式H++OH-===H2O所对应的两个不同类型化学方程式。
①________________________________________________________________________;
②________________________________________________________________________。
(2)在下列反应中:
A.2F2+2H2O===4HF+O2
B.2Na+2H2O===2NaOH+H2↑
C.CaO+H2O===Ca(OH)2
D.2H2O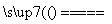 2H2↑+O2↑
2H2↑+O2↑
水只做氧化剂的是________,水只做还原剂的是________,水既做氧化剂又做还原剂的是________,水既不做氧化剂又不做还原剂的是________。请用单线桥法表示B反应的电子转移方向和数目________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com