
反应A+B→C(△t<0)分两步进行:① A+B→X (△H >0)② X→C(△H<0),下列示意图中,能正确表示总反应过程中能量变化的是

 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2016-2017学年河北省高二上第二次月考化学试卷(解析版) 题型:选择题
已知:4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H=-1025kJ/mol,该反应是一个可逆反应。若反应物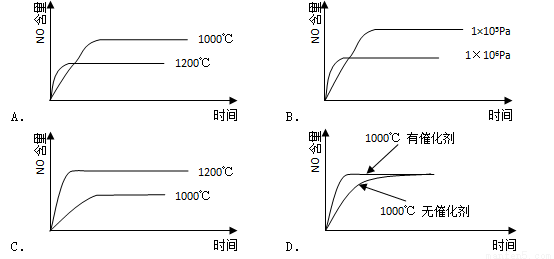
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高二下期初摸底化学卷(解析版) 题型:实验题
磷酸亚铁[Fe3(PO4)2·8H2O]为白蓝色晶体,溶于强酸,不溶于水、醋酸和乙醇。主要用于制造磷酸铁锂电池。实验室制备磷酸亚铁的装置示意图、

反应和实验步骤如下。主要反应为:
3FeSO4+2Na2HPO4+2CH3COONa+8H2O=Fe3(PO4)2·8H2O↓+3Na2SO4+2CH3COOH
实验步骤:①在仪器A中先加入抗坏血酸(C6H8O6)稀溶液作底液②向仪器A中,滴入Na2HPO4与CH3COONa混合溶液至pH=4 ③滴入 15.2克FeSO4溶液,最终维持pH=6,充分反应后,静置④进行操作a,干燥得到的磷酸亚铁12.8克。
15.2克FeSO4溶液,最终维持pH=6,充分反应后,静置④进行操作a,干燥得到的磷酸亚铁12.8克。
(1)仪器A的名称是 。
(2)实验中配制FeSO4溶液时,先要对蒸馏水进行的操作是 。
(3)实验中不是将三种溶液直接混合的原因是 ,反应时需不断搅拌,其目的是 。
(4)步骤④进行的操作a是 。
(5)检验磷酸亚铁粗产品中是否混有氢氧化铁杂质的方法是 。
(6)本实验的产率是 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高二上8月考试化学卷(解析版) 题型:实验题
某小组研究影响反应速率的因素。
(1)实验一:探究酸的强弱对酸与镁条反应速率的影响。
①设计实验方案如下表,表中c = mol·L-1。
编号 | 酸的种类 | 酸的浓度/mol·L-1 | 酸的体积/ml | 镁条质量/g |
1 | 醋酸 | 1.0 | 10 | 2.0 |
2 | 盐酸 | c | 10 | 2.0 |
②实验步骤:
(a)检查装置(左图)的气密性后,添加药品;
(b)反应开始后, ;
(c)将所记录的数据转化为曲线图(右图)。
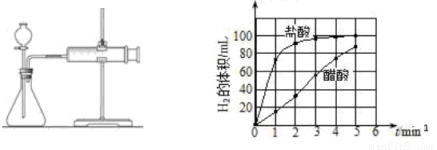
③写出0~5min醋酸、盐酸与镁条反应的反应速率变化规律: 。
(2)实验二:探究反应条件对0.10mol/LNa2S2O3溶液与稀H2SO4反应速率的影响,其设计与测定结果如下:
编号 | 反应温度/℃ | Na2S2O3溶液/ml | V(蒸馏水)/ml | 0.10mol/LH2SO4溶液/ml | 乙 |
1 | 25℃ | 10.0 | 0 | 10.0 | |
2 | 25℃ | 5.0 | a | 10.0 | |
3 | 45℃ | 10.0 | 0 | 10.0 |
I.完成上述实验原理的离子方程式 。
II.上述实验1、3是探究 对化学反应速率的影响;若上述实验1、2是探究浓度对化学反应速率的影响,a为 ;乙是实验需要测量的物理量,则表格中“乙”应填写 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高二上8月考试化学卷(解析版) 题型:选择题
密闭容器中,一定条件下进行如下反应:NO(g)+CO(g) 1/2N2(g)+CO2(g) △H=373.2kJ·mol-1,达到平衡后,为提高反应的速率和NO的转化率,采取的正确措施是
1/2N2(g)+CO2(g) △H=373.2kJ·mol-1,达到平衡后,为提高反应的速率和NO的转化率,采取的正确措施是
A. 加催化剂同时升高温度 B. 加催化剂同时增大压强
C. 升高温度同时充入N2 D. 降低温度同时减小压强
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古高一上第一次月考化学试卷(解析版) 题型:填空题
同温同压下,等质量的SO2与CO2相比较,密度之比为 ,体积之比为_______________
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古高一上第一次月考化学试卷(解析版) 题型:选择题
下列实验仪器不宜直接用来加热的是( )
A. 试管 B. 坩埚 C. 蒸发皿 D. 烧杯
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高二上开学考试化学试卷(解析版) 题型:选择题
有等体积、等pH的Ba(OH)2、KOH和NH3·H2O三种碱溶液,滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为V1、V2、V3,则三者的大小关系正确的是( )
A.V3>V2>V1 B.V3=V2=V1 C.V3>V2=V1 D.V1=V2>V3
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北沙市高二上第一次双周练化学卷(解析版) 题型:选择题
不管化学过程是一步完成或分为数步完成,这个过程的热效应是相同的。
已知:H2O(g)=H2O(l) ΔH1=Q1 kJ·molˉ1;
C2H5OH(g)=C2H5OH(l) ΔH2=Q2 kJ·molˉ1;
C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g) ΔH3=Q3kJ·molˉ1。若使23 g酒精液体完全燃烧,最后恢复到室温,则放出的热量为( )
A.Q1+Q2+Q3 B.0.5(Q1+Q2+Q3)
C.0.5Q1-1.5Q2+0.5Q3 D.-1.5Q1+0.5Q2-0.5Q3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com