
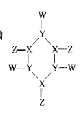
【题目】化合物甲(如图所示)中所有原子都达到了 8电子稳定结构,X、Y、Z、W是原子序数依次增大的短周期主族元素,原子半径:r(w)> r(X)> r(Y) > r(Z)。下列说法正确的是( )
A.YZ,属于酸性氧化物
B.元素的非金属件强弱:Y>Z
C.X的最高价氢化物对应的水化物是强酸
D.Y的最简单氢化物能与W的氢化物反应
【答案】D
【解析】
由结构图可知,W能形成一个键,为H、F或Cl,Y能形成三个键,为N或P,X能形成4个键,为C或Si,Z能形成两个键,为O或S,根据所有原子都达到了 8电子稳定结构,原子半径:r(W)> r(X)> r(Y) > r(Z),可知W为Cl、Y为N、X为C、Z为O。
A. Y为N、Z为O ,YZ为NO,为不成盐的氧化物,不属于酸性氧化物,A错误;
B. Y为N、Z为O ,处于同一周期,从左到右,元素的非金属性增强,所以元素的非金属件强弱:O>N,B错误;
C. X为C ,C的最高价氢化物对应的水化物为H2CO3,是弱酸,C错误;
D. Y为N 、W为Cl,其最简单氢化物分别为:NH3、HCl,NH3与HCl能反应,生成NH4Cl,D正确;故答案为:D。


 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源: 题型:
【题目】下图中a、b、c表示相应仪器中加入的试剂,可用如图装置制取、净化、收集的气体是( )
编号 | 气体 | a | b | c |
|
A | NH3 | 浓氨水 | 生石灰 | 碱石灰 | |
B | CO2 | 盐酸 | 碳酸钙 | 饱和NaHCO3溶液 | |
C | NO | 稀硝酸 | 铜屑 | H2O | |
D | NO2 | 浓硝酸 | 铜屑 | NaOH溶液 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法不正确的是( )

A.将CuSO4溶液蒸发浓缩、冷却结晶可制得胆矾晶体
B.相对于途径①③,途径②更好地体现了绿色化学思想
C.CuSO4在1100℃分解所得气体X可能是SO2和SO3的混合气体
D.Y可能是葡萄糖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于苯的叙述正确的是( )
A.苯的分子式为C6H6,它不能使酸性KMnO4溶液褪色,属于饱和烃
B.从苯的凯库勒式(![]() )看,苯分子中含有碳碳双键,应属于烯烃
)看,苯分子中含有碳碳双键,应属于烯烃
C.在催化剂作用下,苯与液溴反应生成溴苯,发生了加成反应
D.苯分子为平面正六边形结构,6个碳原子之间的价键完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】结合已学知识,并根据下列一组物质的特点回答相关问题。
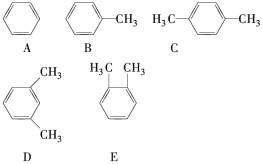
(1)邻二甲苯的结构简式为____(填编号,从A~E中选择)。
(2)A、B、C之间的关系为____(填序号)。
a.同位素 b.同系物 c.同分异构体 d. 同素异形体
(3)请设计一个简单实验来检验A与D,简述实验操作过程:_____________。
(4)有机物同分异构体的熔沸点高低规律是“结构越对称,熔沸点越低”,根据这条规律,判断C、D、E的熔沸点由高到低的顺序:______(填编号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体内缺乏维生素A会使人患夜盲症,原因是维生素A在人体内易被氧化为视黄醛,而视黄醛的缺乏是引起视觉障碍的主要原因。已知视黄醛结构为:

(1)检验分子中醛基的方法是____反应。操作方法____,则证明原溶液中有醛基。
(2)检验分子中碳碳双键的方法是____。
(3)实验中先检验哪种官能团?____试简述理由____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸溶液中存在电离平衡CH3COOH![]() H++CH3COO-,下列叙述不正确的是( )
H++CH3COO-,下列叙述不正确的是( )
A.升高温度,平衡正向移动,醋酸的电离常数Ka值增大
B.0.10mol/L的CH3COOH溶液中加水稀释,溶液中c(OH-)增大
C.CH3COOH溶液中加少量的CH3COONa固体,平衡逆向移动
D.25℃时,欲使醋酸溶液pH、电离常数Ka和电离程度都减小,可加入少量冰醋酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三硫代碳酸钠(Na2CS3)在农业上用作杀菌剂和杀线虫剂,在工业上用于处理废水中的重金属离子。某化学兴趣小组对Na2CS3的一些性质进行探究。回答下列问题:
(1)在试管中加入少量三硫代碳酸钠样品,加水溶解,测得溶液pH=10,由此可知H2CS3是______(填“强”或“弱”)酸。向该溶液中滴加酸性KMnO4溶液,紫色褪去,由此说明Na2CS3具有______性。(填“还原”或“氧化”)。
(2)为了测定某Na2CS3溶液的浓度,按如图装置进行实验。将35.0 mL该Na2CS3溶液置于下列装置A的三颈烧瓶中,打开仪器d的活塞,滴入足量稀硫酸,关闭活塞。
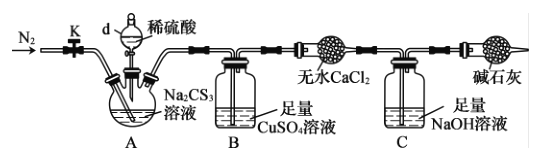
已知:CS32- +2H+==CS2 +H2S↑,CS2 和H2S均有毒;CS2不溶于水,沸点46°C,与CO2某些性质相似,与NaOH作用生成Na2COS2和H2O。
①仪器d的名称是__________。反应开始时需要先通入一段时间N2,其作用为______。
②B中发生反应的离子方程式是________。
③反应结束后。打开活塞K。再缓慢通入热N2(高于60°C)一段时间,其目的是__________。
④为了计算该Na2CS3溶液的浓度,可测定B中生成沉淀的质量。称量B中沉淀质量之前,需要进行的实验操作名称是过滤、_____、________;若B中生成沉淀的质量为8.4g,则该Na2CS3溶液的物质的量浓度是___________。
⑤若反应结束后将通热N2改为通热空气(高于60°C),通过测定C中溶液质量的增加值来计算三硫代碳酸钠溶液的浓度时,计算值______(填“偏高”“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将等浓度的NaOH溶液分别滴加到等pH、等体积的HA、HB两种弱酸溶液中,溶液的pH与粒子浓度比值的对数关系如图所示。下列叙述错误的是( )
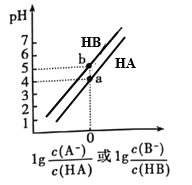
A. a点时,溶液中由水电离的c(OH-)约为1×10-10 mol·L-1
B. 电离平衡常数:Ka(HA)< Ka(HB)
C. b点时,c(B-)=c(HB)>c(Na+)>c(H+)>c(OH-)
D. 向HB溶液中滴加NaOH溶液至pH=7时:c(B-)> c(HB)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com