
某工业生产的废渣中有 CuCO3、Al2O3、Fe3O4、SiO2,现利用下列流程实验废弃物再利用:
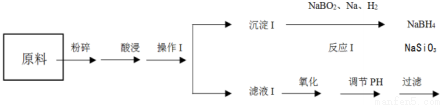

(1)操作Ⅰ所需玻璃仪器有:________________________;
(2)反应Ⅰ的产物NaBH4是有机合成常见的还原剂,该反应的还原剂为________,调节pH 的目的:________________________________;
(3)沉淀2为_____________,高铁酸钠(Na2FeO4)与明矾净水的主要区别为:________________;
(4)若原料中CuCO3和Al2O3的 物质的量之比为1:1,为了提高原料利用率,则试剂x的选择可以为( )
A.CuO B.NaOH C.NH3·H2O D.Cu2(OH)2CO3
(5)CuAlO2是一种新型无机材料,已知反应Ⅱ中还生产一种具有助燃性气体单质,写出反应Ⅱ的化学方程式:______________________;
(6)废弃物中Al2O3的物质的量为1mol,最终制得CuAlO2的质量为184.5g,该制备流程的产率为_______。
 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源:2015-2016学年河北省冀州市高一下期末理科化学A卷(解析版) 题型:选择题
烯烃在一定条件下发生氧化反应,碳碳双键断裂,如:R1CH=CHR2
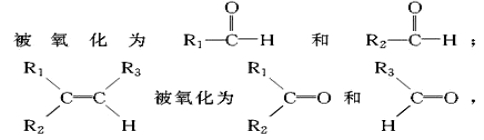
由此推断分子式为C4H8的烯烃的氧化产物有 ( )
A.2种 B.3种 C.4种 D.6种
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高二下第二次月考化学试卷(解析版) 题型:选择题
短周期主族元素X、Y、Z、W的原子序数依次增大,X是形成化合物种类最多的元素,Y原子最外层电子数是其内层电子数的2倍,W是地壳中含量最多的元素。下列叙述正确的是
A. Y与W可以组成YW32-、Y2W42-
B. 由X、Y、Z、W四种元素组成的既能与酸又能与碱反应的化合物,一定属于α-氨基酸
C. 若化合物Y2X4W2能发生银镜反应,则该化合物一定是甲酸甲酯
D. 混合物Y7X8、Y3X8W3中X的质量分数约为8.7%
查看答案和解析>>
科目:高中化学 来源:2016届吉林省长春十一高三下考前冲刺理综化学试卷二(解析版) 题型:实验题
ClO2与Cl2的氧化性相近。在自来水消毒和果蔬保鲜等方面应用广泛。某兴趣小组通过图1装置(夹持装置略)对其制备、吸收、释放和应用进行了研究。
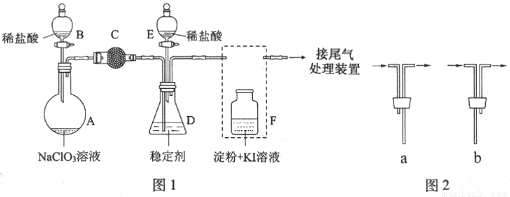
(1)仪器D的名称是___________,安装F中导管时,应选用图2中的___________。
(2)打开B的活塞,A中发生反应:2NaClO3+4HCl═2ClO2↑+Cl2↑+2NaCl+2H2O。为使ClO2在D中被稳定剂充分吸收,滴加稀盐酸的速度宜___________(填“快”或“慢”).
(3)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2,此时F中溶液的颜色不变,则装置C的作用是___________。
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为___________,在ClO2释放实验中,打开E的活塞,D中发生反应,则装置F的作用是___________。
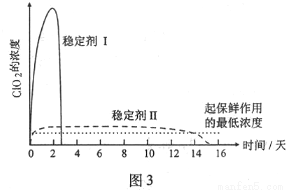
(5)已吸收ClO2气体的稳定剂Ⅰ和稳定剂Ⅱ,加酸后释放ClO2的浓度随时间的变化如图3所示,若将其用于水果保鲜,你认为效果较好的稳定剂是___________,原因是___________。
查看答案和解析>>
科目:高中化学 来源:2016届吉林省长春十一高三下考前冲刺理综化学试卷二(解析版) 题型:选择题
下列说法不正确的是( )
A.利用二氧化碳制造全降解塑料,可以减缓二氧化碳对环境的影响
B.淀粉、油脂、蛋白质都能在人体内水解,也能在体内氧化提供能量
C.CO2与SiO2都是ⅣA族元素的氧化物,但它们的物理性质特别是在熔沸点、硬度上相差很大,这是由于它们的化学键类型不同造成的
D.酸碱质子理论认为,凡能给出质子(H+)的物质都是酸,凡能接受质子的物质都是碱.根据这一理论,Al(OH)3、NaHCO3都是酸碱两性物质
查看答案和解析>>
科目:高中化学 来源:2016届安徽省高三毕业班最后一卷理综化学试卷(解析版) 题型:选择题
常温下,在0.2mol/LAlCl3溶液中,逐滴加入1.0mol/LNaOH溶液,实验测得溶液pH随NaOH溶液体积变化曲线如下图,下列有关说法正确的( )
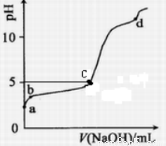
A.a 点时,溶液呈酸性的原因是Al3+水解,离子方程式为:Al3++3OH- Al(OH)3
Al(OH)3
B.b点水的电离程度小于a点
C.通过曲线变化,可估计约为1×10-20
D.d点时,溶液中已无沉淀剩余
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二5月月考化学试卷(解析版) 题型:实验题
工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁[Fe(OH)SO4]的工艺流程如下:

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如下表:
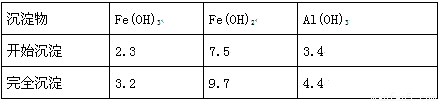
回答下列问题:
(1)加入过量废铁屑的目的是________________________(用离子方程式表示);加入少量NaHCO3的目的是________________________;该工艺中“搅拌”的作用是________________________;
(2)反应Ⅱ中的离子方程式为__________;该流程中可以循环、回收利用的物质是________;
(3)生产中碱式硫酸铁溶液蒸发时需要在减压条件下的原因是________;
(4)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁.根据我国质量标准,产品中不得含有Fe2+及NO3-;为检验所得产品中是否含有Fe2+,应使用的试剂为______。(填写字母)
A.酸性KMnO4溶液 B.KSCN溶液 C.氯水D.NaOH溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二5月月考化学试卷(解析版) 题型:选择题
新版人民币的发行引发了人们对有关人民币中化学知识关注。下列表述不正确的是
A.制造人民币所用的棉花、优质针叶木等原料的主要成分是纤维素
B.用于人民币票面文字等处的油墨中所含有的Fe3O4是一种磁性物质
C.防伪荧光油墨由颜料与树脂连接料等制成,其中树脂属于有机高分子材料
D.某种验钞笔中含有碘酒溶液,遇假钞呈现蓝色,其中遇碘变蓝的是葡萄糖
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高一下第二次月考化学试卷(解析版) 题型:选择题
今有如下三个热化学方程式:
2H2(g)+O2(g)=2H2O(g) 放热Q1 kJ
2H2(g)+O2(g)=2H2O(l) 放热Q2 kJ
H2(g)+1/2O2(g)=H2O(g) 放热Q3 kJ ,其中Q1 Q2 Q3 大小关系是( )
A.Q1=Q2=Q3 B.2Q3=Q1<Q2 C.Q3<Q2<Q1 D.Q1<Q2<3Q3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com