
| A£® | ¢Ł¢Ś¢Ü¢Ż | B£® | ¢Ś¢Ū¢Ü | C£® | ¢Ś¢Ü¢Ż | D£® | ¢Ū¢Ü¢Ż |
·ÖĪö ¢ŁPM2.5ŹĒĪ¢Į£Ö±¾¶ĪŖ2.5Ī¢Ć×µÄæÅĮ££¬1Ī¢Ć×=1000nm£¬½įŗĻ½ŗĢåĪ¢Į£Ö±¾¶“óŠ”·ÖĪö£»
¢Ś“æ¼īĪŖĢ¼ĖįÄĘ£¬½įŗĻĢ¼ĖįÄĘ×é³É·ÖĪö£»
¢ŪČÜŅŗµ¼µēŠŌÓė“ųµēŗɵĥė×ÓÅØ¶Č“óŠ”ĪŽ¹Ų£¬ĒāŃõ»ÆÄĘČÜŅŗµÄµ¼µēÄÜĮ¦²»Ņ»¶Ø±Č°±Ė®ČÜŅŗĒ棻
¢Ü½ŗĢå¾ßÓŠ¶”“ļ¶ūŠ§Ó¦£¬ŌĘ”¢Īķ¶¼ŹōÓŚ½ŗĢ壻
¢ŻøÖĢśøÆŹ“Ź±øŗ¼«ĢśŹ§Č„µē×ÓÉś³ÉŃĒĢśĄė×Ó£®
½ā“š ½ā£ŗ¢ŁPM2.5ŹĒĪ¢Į£Ö±¾¶ĪŖ2.5Ī¢Ć×µÄæÅĮ££¬1Ī¢Ć×=1000nm£¬”°PM2.5”±ŹĒĻøŠ”æÅĮ£ĪļŠüø”ŌŚæÕĘųÖŠŠĪ³ÉµÄ²»ŹĒ½ŗĢ壬¹Ź¢Ł“ķĪó£»
¢Ś“æ¼īĪŖĢ¼ĖįÄʵÄĖ×³Ę£¬Ģ¼ĖįÄĘ¼ČŹōÓŚÕżŃĪÓÖŹōÓŚÄĘŃĪŗĶĢ¼ĖįŃĪ£¬¹Ź¢ŚÕżČ·£»
¢ŪČÜŅŗµ¼µēŠŌÓėČÜŅŗÖŠŅõŃōĄė×ÓÅضČÓŠ¹Ų£¬ŌņĻąĶ¬ĪĀ¶ČĻĀĒāŃõ»ÆÄĘČÜŅŗµÄµ¼µēÄÜĮ¦²»Ņ»¶Ø±Č°±Ė®Ē棬¹Ź¢Ū“ķĪó£»
¢Ü½ŗĢåÓĆŅ»ĖŁ¹āÕÕÉä»įÓŠ¹āĮĮµÄĶØĀ·£¬ĖłŅŌæÉŅŌĒų±šČÜŅŗÓė½ŗĢ壬ŌĘ”¢ĪķŹĒĘųČܽŗ£¬¹Ź¢ÜÕżČ·£»
¢ŻøÖĢśµÄĪüŃõøÆŹ“ÖŠ£¬øŗ¼«FeŹ§Č„µē×ÓÉś³ÉŃĒĢśĄė×Ó£¬Ęäøŗ¼«·¢Éś·“Ó¦ĪŖ£ŗFe-2e-ØTFe2+£¬¹Ź¢ŻÕżČ·£»
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²é½ĻĪŖ×ŪŗĻ£¬Éę¼°ĪļÖŹ·ÖĄą”¢½ŗĢåŠŌÖŹ”¢»·¾³ĪŪČ¾”¢½šŹōøÆŹ“”¢ČÜŅŗµ¼µēŠŌµČÖŖŹ¶£¬ĢāÄæÄѶČÖŠµČ£¬×¢ŅāÕĘĪÕ³£¼ūĪļÖŹ×é³É”¢½į¹¹ÓėŠŌÖŹ£¬Ć÷Č·½ŗĢåŠŌÖŹ”¢½šŹōøÆŹ“ŌĄķ£¬ŹŌĢāÅąŃųĮĖѧɜµÄ·ÖĪöÄÜĮ¦¼°Įé»īÓ¦ÓĆÄÜĮ¦£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | SO3µÄÉś³ÉĖŁĀŹµČÓŚĖüµÄĻūŗÄĖŁĀŹ | B£® | v£ØSO2£©Õż=2v£ØO2£©Äę | ||
| C£® | ø÷×é·ÖµÄ·“Ó¦ĖŁĀŹ¾łĻąµČ | D£® | ·“Ó¦ĢåĻµÖŠ»ģŗĻĪļµÄ×é³É±£³Ö²»±ä |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Õż³£ÓźĖ®pHµČÓŚ7£¬ĖįÓźµÄPHŠ”ÓŚ7 | |
| B£® | ½šŹōÄĘ×Å»šČ¼ÉÕŹ±£¬ÓĆÅŻÄĆš»šĘ÷Ćš»š | |
| C£® | ĀĮ±ČĢś»īĘĆ£¬ĖłŅŌĀĮ±ČĢśøüČŻŅ×±»øÆŹ“ | |
| D£® | CO2ĶØČėæÉČÜŠŌ¹čĖįŃĪÖŠĪö³ö¹čĖį³Įµķ£¬ĖłŅŌ¹čĖįµÄĖįŠŌŠ”ÓŚĢ¼Ėį |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
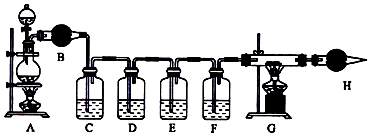
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
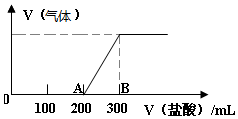 Ļņ100mL1.5mol/LµÄ±ūČÜŅŗÖŠ»ŗĀżĶØČėŅ»¶ØĮæµÄCO2£¬³ä·Ö·“Ó¦ŗó£¬ĻņĖłµĆČÜŅŗÖŠÖšµĪ»ŗĀżµĪ¼Ó0.5mol/LµÄŃĪĖį£¬ĖłµĆĘųĢåµÄĢå»żÓėĖł¼ÓŃĪĖįµÄĢå»ż£Ø²»æ¼ĀĒĘųĢåČܽāÓŚĖ®£©¹ŲĻµČēĶ¼ĖłŹ¾£®
Ļņ100mL1.5mol/LµÄ±ūČÜŅŗÖŠ»ŗĀżĶØČėŅ»¶ØĮæµÄCO2£¬³ä·Ö·“Ó¦ŗó£¬ĻņĖłµĆČÜŅŗÖŠÖšµĪ»ŗĀżµĪ¼Ó0.5mol/LµÄŃĪĖį£¬ĖłµĆĘųĢåµÄĢå»żÓėĖł¼ÓŃĪĖįµÄĢå»ż£Ø²»æ¼ĀĒĘųĢåČܽāÓŚĖ®£©¹ŲĻµČēĶ¼ĖłŹ¾£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Čō»ģŗĻŗóČÜŅŗÖŠc£ØH+£©£¾c£ØOH-£©£¬ŌņŅ»¶ØÓŠV1£¼V2 | |
| B£® | ČōV1=V2£¬Ōņ¶žÕß»ģŗĻŗóµÄČÜŅŗÖŠpH£¾7 | |
| C£® | »ģŗĻČÜŅŗÖŠæÉÄÜ“ęŌŚ£ŗc £Ø F-£©£¾c £ØH+£©£¾c £ØNa+£©£¾c£Ø OH-£© | |
| D£® | ¶žÕßĒ”ŗĆ·“Ó¦ĶźŹ±£¬ŌņĖłµĆČÜŅŗÖŠc£ØF-£©=c £ØNa+£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
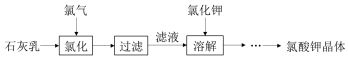
| ¼ÓČČ“ĪŹż | µŚŅ»“Ī | µŚ¶ž“Ī | µŚČż“Ī | µŚĖÄ“Ī |
| Ź£Óą¹ĢĢåÖŹĮæ£Øg£© | c | d | e | e |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
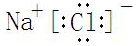 £¬·“Ó¦ÖŠ±»Ńõ»ÆµÄĪļÖŹŹĒFe£ØOH£©3£ØŠ“»ÆѧŹ½£©£®
£¬·“Ó¦ÖŠ±»Ńõ»ÆµÄĪļÖŹŹĒFe£ØOH£©3£ØŠ“»ÆѧŹ½£©£®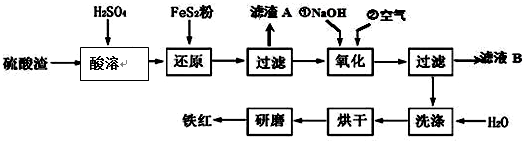
| ³ĮµķĪļ | Fe£ØOH£©3 | Al£ØOH£©3 | Fe£ØOH£©2 | Mg£ØOH£©2 |
| æŖŹ¼³ĮµķpH | 2.7 | 3.8 | 7.6 | 9.4 |
| ĶźČ«³ĮµķpH | 3.2 | 5.2 | 9.7 | 12.4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
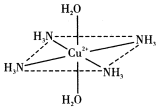 ĶłĮņĖįĶĖ®ČÜŅŗÖŠ¼ÓČė°±Ė®£¬Ź×ĻČÉś³ÉÄŃČÜĪļ£¬¼ĢŠų¼Ó°±Ė®£¬ÄŃČÜĪļČܽā£¬¶ųĒŅĖłµĆČÜŅŗµÄŃÕÉ«±ČŌĄ“Ć÷ĻŌ¼ÓÉī£¬µĆµ½ĮĖŅ»ÖÖŗ¬2+µÄČÜŅŗ£¬“ĖĄė×ÓµÄĮ¢Ģå½į¹¹ČēĶ¼ĖłŹ¾£Ø4øöNH3ÓėCu2+¹²Ćę£¬øśH2O-Cu2+-H2OÖįĻß“¹Ö±£©£®Ēė»Ų“šŅŌĻĀĪŹĢā£ŗ
ĶłĮņĖįĶĖ®ČÜŅŗÖŠ¼ÓČė°±Ė®£¬Ź×ĻČÉś³ÉÄŃČÜĪļ£¬¼ĢŠų¼Ó°±Ė®£¬ÄŃČÜĪļČܽā£¬¶ųĒŅĖłµĆČÜŅŗµÄŃÕÉ«±ČŌĄ“Ć÷ĻŌ¼ÓÉī£¬µĆµ½ĮĖŅ»ÖÖŗ¬2+µÄČÜŅŗ£¬“ĖĄė×ÓµÄĮ¢Ģå½į¹¹ČēĶ¼ĖłŹ¾£Ø4øöNH3ÓėCu2+¹²Ćę£¬øśH2O-Cu2+-H2OÖįĻß“¹Ö±£©£®Ēė»Ų“šŅŌĻĀĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com