
下列说法正确的是
A.置换反应一定属于氧化还原反应 B.分解反应均不属于氧化还原反应
C.复分解反应有的属于氧化还原反应 D.化合反应有的属于氧化还原反应
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016届云南省高三上学期第一次月考化学试卷(解析版) 题型:选择题
在一定条件下,按下列物质的量关系进行反应,其对应的离子方程式或化学方程式书写正确的是
A.n(Cl2)∶n(Fe)=5∶4 5Cl2+4Fe 2FeCl2+2FeCl3
2FeCl2+2FeCl3
B.n(Cl2)∶n(FeBr2)=1∶1 Fe2++2Br-+Cl2=Fe3++Br2+2Cl-
C.n(MnO4-)∶n(H2O2)=2∶3 2MnO4-+3H2O2+6H+=2Mn2++4O2↑+6H2O
D.n(Fe)∶n[HNO3(稀)]=1∶3 4Fe+12H++3NO3-===3Fe2++Fe3++3NO↑+6H2O
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省高二开学考试化学试卷(解析版) 题型:选择题
原电池反应是释放能量的氧化还原反应,下列可设计成原电池的化学反应是
A.H2O (l)+CAO(s)=CA(OH)2(s)
B.BA(OH)2·8H2O+2NH4Cl=BACl2+2NH3·H2O+8H2O
C.2KClO3 2KCl+3O2↑
2KCl+3O2↑
D.CH4(g)+2O2(g)=CO2(g)+2H2O(l)
查看答案和解析>>
科目:高中化学 来源:2016届湖南省衡阳市高三上学期第一次月考化学试卷(解析版) 题型:选择题
已知氧化还原反应:2Cu(IO3)2+24KI+12H2SO4===2CuI↓+13I2+12K2SO4+12H2O
其中1 mol氧化剂在反应中得到的电子为
A.10 mol B.11 mol C.12 mol D.13 mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高一入学摸底化学试卷(解析版) 题型:填空题
(8分)有一包白色固体混合物,该混合物可能含有CuSO4、Na2CO3、Na2SO4、MgCl2,现进行如下实验:
(1)将混合物溶于水,得到无色透明溶液。
(2)取上述溶液分成两份盛于试管中,其中一份滴加BaCl2溶液,产生白色沉淀,再加稀硝酸,沉淀不溶解;另一份滴加NaOH溶液,有白色沉淀生成。试根据实验现象推断,并完成下面的填空:
该混合物中肯定没有________和________;肯定含有________和________(写化学式)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高二9月检测化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.油脂是高级脂肪酸的甘油酯
B.油脂与氢气发生加成反应,可以得到硬化油
C.油脂在酸性条件或碱性条件下,可以发生皂化反应
D.日常使用的花生油、豆油、动物油都是油脂,它们可以溶解一些脂溶性维生素
查看答案和解析>>
科目:高中化学 来源:2016届四川省高三9月月考化学试卷(解析版) 题型:实验题
(14分)铜在自然界存在于多种矿石中.
(Ⅰ)以硅孔雀石(主要成 分为CuSiO3•2H2O,含少量SiO2、FeCO3、Fe2O3等杂质)为原料制取硫酸铜的工艺流程如下:
分为CuSiO3•2H2O,含少量SiO2、FeCO3、Fe2O3等杂质)为原料制取硫酸铜的工艺流程如下:
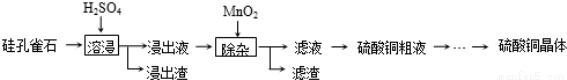
已知:Fe3+、Cu2+和Fe2+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、6.7和9.7.
(1)“溶浸”中CuSiO3•2H2O和H2SO4发生反应的化学方程式 .
(2)“溶浸”中,选取浓度为20% H2SO4为浸出剂,铜的浸出率与浸出时间的关系见图1.由图1可得,随着浸出时间的增长, (至少写一条变化规律).

(3)“除杂”中,加入MnO2的作用是 (用离子方程式表示).“除杂”中需在搅拌下加入石灰乳以调节溶液的pH到3~4,沉淀部分杂质离子,分离得滤液.滤渣的主要成分为 .
(Ⅱ)以黄铜矿(主要成分为CuFeS2)为原料炼制精铜的工艺流程如下:
黄铜矿 精铜冰铜(Cu2S和FeS)
精铜冰铜(Cu2S和FeS) 粗铜
粗铜 精铜
精铜
(4)“还原”工艺中其中一个反应为:Cu2S+2Cu2O  6Cu+SO2↑,该反应的氧化剂是 .
6Cu+SO2↑,该反应的氧化剂是 .
(5)粗铜含少量Fe、Ag、Au等金属杂质,电解精炼铜时,阴极反应式为 .完成图2中由粗铜电解得到精铜 的示意图,并作相应标注.
的示意图,并作相应标注.

查看答案和解析>>
科目:高中化学 来源:2016届江西省高三上学期第一次月考化学试卷(解析版) 题型:选择题
利用下列各组物质制备和收集少量相应气体,能采用下图实验装置的是
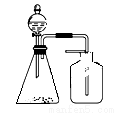
A.FeS与稀硫酸 B.铜与浓硫酸
C.稀硝酸与铜片 D.电石与水
查看答案和解析>>
科目:高中化学 来源:2016届四川省高三9月月考化学试卷(解析版) 题型:填空题
[化学—选修3:物质结构与性质](15分)早期发现的一种天然准晶颗粒由三种Al、Cu、Fe元素组成。回答下列问题:
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过 方法区分晶体、准晶体和非晶体。
(2)基态铁原子有 个未成对电子,三价铁离子的电子排布式为: ,可用硫氰化钾检验三价铁离子,形成配合物的颜色为 。
(3)新制备的氢氧化铜可将乙醛氧化为乙酸,而自身还原成氧化亚铜,乙醛中碳原子的杂化轨道类型为 ,一摩尔乙醛分子中含有的σ键的数目为 。乙酸的沸点明显高于乙醛,其主要原因是: 。氧化亚铜为半导体材料,在其立方晶胞内部有四个氧原子,其余氧原子位于面心和顶点,则该晶胞中有 个铜原子。
(4)铝单质为面心立方晶体,其晶胞参数a=0.405nm(晶胞参数就是晶胞立方体的边长),晶胞中铝原子的配位数为 。列式表示铝单质的密度 g·cm-3(不必计算出结果)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com