

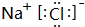 ,故答案为:
,故答案为: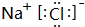 .
.


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:
| A、水电离的c(H+)=1×10-13mol/L的溶液中:Na+、Ba2+、Cl-、NO3- |
| B、使酚酞变红色的溶液:Na+、Cu2+、HCO3-、NO3- |
| C、在酸性条件下:Fe2+、Cl-、NO3-、K+ |
| D、在无色溶液中:Al3+、Cl-、K+、AlO2- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 主 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ? | ? |
查看答案和解析>>
科目:高中化学 来源: 题型:
 A、B、C三种短周期元素在周期表中相对位置如表格:
A、B、C三种短周期元素在周期表中相对位置如表格:| A | |||
| B | C |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
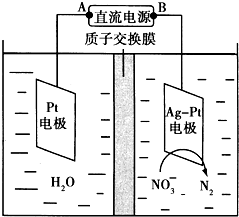 化学在环境保护中起着十分重要的作用.催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染.
化学在环境保护中起着十分重要的作用.催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染.
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、水电离出来的c(H+)=10-13mol/L的溶液中K+、Cl-、NO3-、I- |
| B、强酸性溶液中:Al3+、K+、Mg2+、Cl-、SO42- |
| C、c(Fe3+)=0.1mol?L-1的溶液中:Na+、SCN-、Cl-、Br- |
| D、强碱性溶液中:ClO-、SO42-、SO32-、Na+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com