
【题目】煤制天然气工艺是煤高效洁净利用的新途径之一,其工艺流程简如图1如下:
(1)反应I:C(s)+H2O(g)CO(g)+H2(g)△H=+135kJmol﹣1 , 通入的氧气会与部分碳发生燃烧反应.请利用能量转化及平衡移动原理说明通入氧气的作用: .
(2)反应II:CO(g)+H2O(g)CO2(g)+H2(g)△H=﹣41kJmol﹣1 . 如图2表示不同温度条件下,煤气化反应I发生后的汽气比(水蒸气与原料气中CO物质的量之比)与CO平衡转化率的变化关系.
①判断T1、T2和T3的大小关系: .
②若煤气化反应I发生后的汽气比为0.8,经煤气化反应I和水气变换反应II后,得到CO与H2的物质的量之比为1:3,则反应II应选择的温度是(填“T1”“T2”或“T3”).
(3)①甲烷化反应IV发生之前需要进行脱酸反应III.煤经反应I和II后的气体中含有两种酸性气体,分别是H2S和 .
②工业上常用热碳酸钾法脱除H2S气体得到两种酸式盐,该反应的化学方程式是 .
(4)已知:
CO(g)+H2O(g)CO2(g)+H2(g)△H1=﹣41kJmol﹣1
2H2(g)+O2(g)2H2O(g)△H2=﹣484kJmol﹣1
CH4(g)+2O2(g)CO2(g)+2H2O(g)△H3=﹣802kJmol﹣1
反应IV:CO(g)+3H2(g)CH4(g)+H2O(g)△H=
【答案】
(1)氧气与碳发生燃烧反应放热,放出的热被可逆反应C(s)+H2O(g)?CO(g)+H2(g)吸收利用,促进反应正向移动
(2)T1<T2<T3;T3
(3)CO2;K2CO3+H2S═KHS+KHCO3
(4)﹣207kJ?mol﹣1
【解析】解:(1)C(s)+H2O(g)CO(g)+H2(g)△H=+135kJmol﹣1 , 是吸热反应,而碳与氧气反应放出热量,使反应C(s)+H2O(g)CO(g)+H2(g),向正反应方向移动,提高碳的利用率,
所以答案是:氧气与碳发生燃烧反应放热,放出的热被可逆反应C(s)+H2O(g)CO(g)+H2(g)吸收利用,促进反应正向移动;(2)①反应CO(g)+H2O(g)CO2(g)+H2(g)△H=﹣41kJmol﹣1的正反应为放热反应,温度越高一氧化碳的转化率越低,由图可知,温度的大小为:T1<T2<T3 , 所以答案是:T1<T2<T3;
②若煤气化反应I发生后的汽气比为0.8,设水蒸气的物质的量是4mol、则生成的CO物质的量为5mol,同时生成5mol氢气,经煤气化反应I和水气变换反应II后,设反应II中CO转化的为xmol,则生成xmol氢气,则(5﹣x):(5+x)=1:3,x=2.5,CO的转化率= ![]() ×100%=50%,根据图知,反应温度为T3 ,
×100%=50%,根据图知,反应温度为T3 ,
所以答案是:T3;(3)①根据方程式II知,生成的酸性气体还有二氧化碳,所以答案是:CO2;
②工业上常用热碳酸钾法脱除H2S气体得到两种酸式盐,则二者反应生成碳酸氢钾和硫氢化钾,反应方程式为K2CO3+H2S═KHS+KHCO3 ,
所以答案是:K2CO3+H2S═KHS+KHCO3;(4)CO(g)+H2O(g)CO2(g)+H2(g)△H1=﹣41kJmol﹣1 ①
2H2(g)+O2(g)2H2O(g)△H2 =﹣484kJmol﹣1 ②
CH4(g)+2O2(g)CO2(g)+2H2O(g)△H3=﹣802kJmol﹣1 ③
将方程式①+2②﹣③得反应IV:CO(g)+3H2(g)CH4(g)+H2O(g)△H=△H1+2△H2﹣△H3=(﹣41kJmol﹣1)+2(﹣484kJmol﹣1 )﹣(﹣802kJmol﹣1)=﹣207 kJmol﹣1 ,
所以答案是:﹣207 kJmol﹣1 .
【考点精析】本题主要考查了化学平衡状态本质及特征和化学平衡的计算的相关知识点,需要掌握化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效);反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%才能正确解答此题.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:
【题目】铁炭混合物(铁屑和活性炭的混合物)、纳米铁粉均可用于处理水中污染物.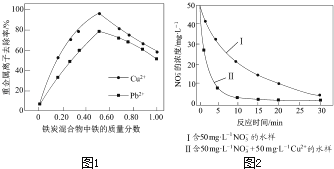
(1)铁炭混合物在水溶液中可形成许多微电池.将含有Cr2O72﹣的酸性废水通过铁炭混合物,在微电池正极上Cr2O72﹣转化为Cr3+ , 其电极反应式为 .
(2)在相同条件下,测量总质量相同、铁的质量分数不同的铁炭混合物对水中Cu2+和Pb2+的去除率,结果如图1所示.
①当铁炭混合物中铁的质量分数为0时,也能去除水中少量的Cu2+和Pb2+ , 其原因是 .
②当铁炭混合物中铁的质量分数大于50%时,随着铁的质量分数的增加,Cu2+和Pb2+的去除率不升反降,其主要原因是 .
(3)纳米铁粉可用于处理地下水中的污染物.
①一定条件下,向FeSO4溶液中滴加碱性NaBH4溶液,溶液中BH4﹣(B元素的化合价为+3)与Fe2+反应生成纳米铁粉、H2和B(OH)4﹣ , 其离子方程式为 .
②纳米铁粉与水中NO3﹣反应的离子方程式为:4Fe+NO3﹣+10H+═4Fe2++NH4++3H2O。
研究发现,若pH偏低将会导致NO3﹣的去除率下降,其原因是 .
③相同条件下,纳米铁粉去除不同水样中NO3﹣的速率有较大差异(见图2),产生该差异的可能原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示物质结构的化学用语或说法中,正确的是( )
A.中子数为8的氮原子:8N
B.次氯酸的电子式: ![]()
C.PCl5分子的每个原子都满足8电子稳定结构
D.用电子式表示NaCl的形成过程: ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.大米富含淀粉
B.加碘食盐含有碘酸钾(KIO3)
C.人体必需的微量元素就是维生素
D.人体必需的微量元素不都是金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用如图装置完成下表所列的四个实验,不能达到实验目的是( )
选项 | 实验目的 | 试剂X | 试剂Y |
A | 验证C2H5OH与浓H2SO4加热至170℃制得的乙烯的性质 | NaOH溶液 | Br2水 |
B | 检验FeSO4受热分解产生的气体中由SO3和SO2 | BaCl2溶液 | 品红溶液 |
C | 验证电石与饱和食盐水反应生成的乙炔的性质 | CuSO4溶液 | KMnO4溶液 |
D | 验证氧化性:Cl2>Br2>I2 | NaBr溶液 | KI溶液 |
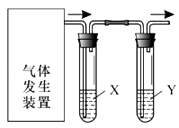
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化银胶体中的分散质粒子实际上是一个个由很多“AgCl”结合而成的集合体.向盛有NaCl溶液的试管中滴加AgNO3溶液,静置后用一束光照射试管,发现试管的三个不同区域中只有一个区域具有明显的丁达尔效应,则下列分析正确的是( ) 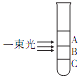
A.该区域是A,该区域中AgCl的直径最小
B.该区域是B,该区域中AgCl的直径介于
A.C区域之间
B.该区域是C,该区域中AgCl的直径最大
C.各区域AgCl的大小都相同,但只有B区域中分散质的大小介于1~100 nm之间
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大;A是周期表中原子半径最小的元素;B元素的最高价氧化物的水化物与其简单氢化物能相互反应生成盐;C元素原子的最外层电子数是内层电子数的3倍;D元素的主族序数等于其周期数;E元素原子的最外层电子数是其电子层数的2倍.G单质是日常生活中用量最大的金属,易被腐蚀. 试回答下列问题:
(1)A元素的同位素有(写原子符号)
(2)实验室制取B的简单氢化物的化学反应方程式为
(3)C,D,E,F的简单离子半径由大到小的顺序是(用离子符号表示)
(4)用化学事实说名E与F这两种元素非金属性的强弱(举一例)
(5)下列有关G的说法不正确的是 A、铁位于第四周期ⅧB族,在人体内的血红蛋白中含有铁元素
B、过量的铁分别与氯气和稀盐酸反应所得氯化物相同
C、FeCl3、FeCl2、Fe(OH)3都可以通过化合反应制取
D、氢氧化铁与HI溶液仅发生中和反应
(6)向NaOH溶液中通入一定量的F单质,两者恰好完全反应,生成物中有三种含F的离子,其中两种离子的物质的量与反应时间的曲线如图所示.请写出t2时反应的总的化学方程式 . 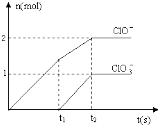
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学--选修2:化学与技术]高锰酸钾(KMnO4)是一种常用氧化剂,主要用于化工、防腐及制药工业等.以软锰矿(主要成分为MnO2)为原料生产高锰酸钾的工艺路线如下:
回答下列问题:
(1)原料软锰矿与氢氧化钾按1:1的比例在“烘炒锅”中混配,混配前应将软锰矿粉碎,其作用是 .
(2)“平炉”中发生的化学方程式为 .
(3)“平炉”中需要加压,其目的是 .
(4)将K2MnO4转化为KMnO4的生产有两种工艺.
①“CO2歧化法”是传统工艺,即在K2MnO4溶液中通入CO2气体,使体系呈中性或弱碱性,K2MnO4发生歧化反应,反应中生成KMnO4 , MnO2和(写化学式).
②“电解法”为现代工艺,即电解K2MnO4水溶液,电解槽中阳极发生的电极反应为
, 阴极逸出的气体是 .
③“电解法”和“CO2歧化法”中,K2MnO4的理论利用率之比为 .
(5)高锰酸钾纯度的测定:称取1.0800g样品,溶解后定容于100mL容量瓶中,摇匀.取浓度为0.2000molL﹣1的H2C2O4标准溶液20.00mL,加入稀硫酸酸化,用KMnO4溶液平行滴定三次,平均消耗的体积为24.48mL,该样品的纯度为(列出计算式即可,已知2MnO4﹣+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com