
【题目】请按要求回答问题。
(1)Si的基态原子核外电子排布式____,S的基态原子核外有____个未成对电子
(2)用“<”“>”填空
离子半径 | 电负性 | 熔点 | 酸性 |
O2-____Na+ | N___O | 金刚石_____晶体硅 | 硫酸___高氯酸 |
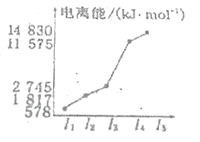
(3)第三周期某元素的电离能情况如图所示,则该元素位于元素周期表第____列
(4)Mn、Fe均为第4周期的过渡元素,两元素的部分电离能数据列于下表:
元素 | Mn | Fe | |
电离能/kJ·mol-1 | I1 | 717 | 759 |
I2 | 1509 | 1561 | |
I3 | 3248 | 2957 | |
比较两元素的I2、I3可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难,对此,你的解释是______。
(5)下图能表示HF分子形成的是(____)
a.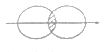 b.
b.![]()
c.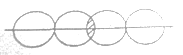 d.
d.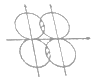
【答案】1s22s22p63s23p2 2 > < > < 13 Mn2+的价电子排布式为3d5,原子轨道处于半满状态,能量低更稳定,而Fe2+的价电子排布式为3d6,3d能级有6个电子,失去一个电子就达到3d5半充满稳定结构,故Fe2+容易再失去一个电子 b
【解析】
(1)Si是14号元素,其基态原子核外电子排布式1s22s22p63s23p2,S为16号元素,其基态原子核外电子排布式1s22s22p63s23p4,有2个未成对电子;答案:1s22s22p63s23p2;2。
(2)电子层结构相同的离子,核电荷数越大离子半径越小,故离子半径:O2->Na+;同周期自左而右,元素电负性增大,所以电负性N<O;金刚石与晶体硅均属于原子晶体,C原子半径较小,键长更短,故C-C键更稳定,熔沸点金刚石>晶体硅;非金属性S<Cl,非金属性越强,最高价含氧酸的酸性越强,故酸性:H2SO4<HClO4,因此,本题正确答案是:>;<;>;<。
(3)由图表可知该元素的各级电离能逐级增大,I1和I2、I3差别较小,但I4I3,I4突跃式变大,即失去3个电子后,再失去电子变为+4价阳离子非常困难,该元素的核外电子排布为1s22s22p63s23p1,说明该元素为第IIIA主族,在元素周期表的第13列。答案:13。
(4)原子轨道处于半满、全满、全空时,能量更低、更稳定,Mn2+的价电子排布式为3d5,3d能级有5个电子,为半充满状态,能量低更稳定,所以难再失去一个电子,而Fe2+的价电子排布式为3d6,3d能级有6个电子,失去一个电子就达到3d5半充满稳定结构,故Fe2+容易再失去一个电子。答案:Mn2+的价电子排布式为3d5,原子轨道处于半满状态,能量低更稳定,而Fe2+的价电子排布式为3d6,3d能级有6个电子,失去一个电子就达到3d5半充满稳定结构,故Fe2+容易再失去一个电子。
(5)HF是双原子分子,两个原子共用一对电子形成共价键,键角为180![]() ,因为F的电负性很大,容易形成氢键,氟原子和另外一个分子中的氢原子形成氢键,所以b符合题意;答案:b。
,因为F的电负性很大,容易形成氢键,氟原子和另外一个分子中的氢原子形成氢键,所以b符合题意;答案:b。


科目:高中化学 来源: 题型:
【题目】下图是用0.100 0 mol·L-1 NaOH溶液滴定20.00 mL未知浓度盐酸(酚酞作指示剂)的滴定曲线,下列说法正确的是
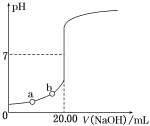
A. 水电离出的氢离子浓度:a<b
B. 盐酸的物质的量浓度为0.010 0 mol·L-1
C. 指示剂变色时,说明盐酸与NaOH恰好完全反应
D. 当滴加NaOH溶液为10.00 mL时,该混合液的pH=1+lg 3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有 X、Y、Z 三种元素,X 是有机化合物中必含的元素, Y 是地壳里含量最多的元素,Z 是质量最轻的元素。X、Y、Z 三种元素组成的有机物 M 能被酸性高锰酸钾氧化生成 N。为了测定有机物 M 的结构,做如下实验:
①将 4.6 g 有机物 M 完全燃烧,测得生成 0.2mol CO2 和 5.4 g 水;
②用质谱仪检测有机物 M,得到如图一所示的质谱图;
③用核磁共振仪处理有机物 M,得到如图二所示图谱,图中三个峰面积之比为1:2:3
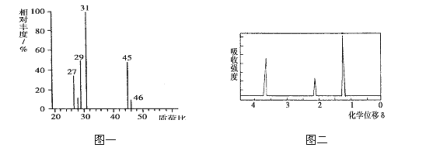
试回答下列问题:
⑴M 的结构简式是______________。
⑵N 中含有的官能团的结构简式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】山梨酸钾是世界公认的安全型食品防腐剂,山梨酸钾的一条合成路线如下图所示。
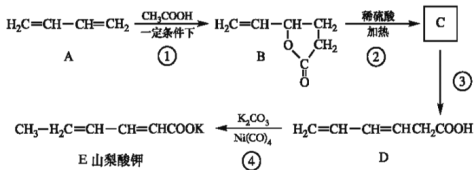
回答下列问题:
(1)B中含氧官能团名称是________。
(2)①的反应的类型是________,③的反应条件是________。
(3)②的反应方程式为_________________________________。
(4)D有多种同分异构体,写出一种符合下列要求或者信息的有机物的结构简式________。
Ⅰ.分子中所有碳原子在一个环上,且只有一个环,Ⅱ.含有三种化学环境不同的氢原子
Ⅲ.当羟基与双键碳原子相连接时,这种结构是不稳定的,易发生如下转化:
![]()
(5)苯甲酸钠(![]() )也是一种重要的防腐剂,写出由甲苯制备苯甲酸钠的合成路线。(其他试剂任选)_____________
)也是一种重要的防腐剂,写出由甲苯制备苯甲酸钠的合成路线。(其他试剂任选)_____________
(合成路线常用的表示方式为:![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值下列有关说法中正确的是( )
A.常温常压下,46gN2O4中含氧原子数为2NA
B.常温常压下,11.2LNH3中含共价键的数目为1.5NA
C.电解精炼铜阳极质量减少32g时电路中转移电子总数为NA
D.1L0.2mol/LNa2SO4溶液中含有阴阳离子总数为0.6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请按要求完成下列各题:
(1)将一小块钠投入到盛CuSO4溶液的烧杯中,剧烈反应,放出气体并生成蓝色沉淀,其反应的离子方程式为___。
(2)将FeSO4溶液与过量NaOH溶液混合并在空气中放置一段时间,整个过程中的现象为___,反应过程分两步,其中第2步反应的化学方程式为___。
(3)写出溶液中硫酸氢钠的电离方程式___。
(4)配制某浓度的稀硫酸,用10mL量筒量取浓硫酸的体积如图Ⅰ所示,A与B,B与C刻度间相差1mL,如果刻度A为8,量筒中浓硫酸的体积是___mL。

(5)要用CuSO4·5H2O晶体配制500mL0.01mol/LCuSO4溶液,应该用托盘天平称取CuSO4·5H2O___g(读到小数点后两位)
(6)图Ⅱ所示仪器的名称是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一无色透明的溶液做如下实验:
①取少量溶液滴加盐酸酸化的BaCl2溶液有白色沉淀生成。
②另取部分溶液加入Na2O2,有无色无味气体放出且有白色沉淀生成,加入Na2O2的量与生成沉淀的量的关系如图所示,试问:
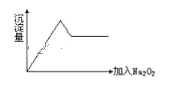
(1)Cu2+、NH4+、Al3+、Mg2+、Na+、Fe3+、K+、SO42-等离子中一定存在的离子是__;可能存在的离子是__;一定不存在的离子是___。
(2)上述溶液至少由___等物质混合成。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用63%的浓HNO3(其密度为1.4g/mL)配制240mL0.50mol/L稀HNO3,若实验仪器有:A.10mL量筒 B.50mL量筒 C.托盘天平 D.玻璃棒 E.100mL容量瓶 F.250mL容量瓶 G.500mL容量瓶 H.胶头滴管 I.200mL烧杯。
(1)此浓硝酸的物质的量浓度为___mol/L。
(2)应量取63%的浓硝酸___mL,应选用的量筒是___(填仪器的字母编号)。
(3)实验时还需选用的仪器有(填序号)D、I、___(填序号)
(4)配制过程中,下列操作会使配制的稀硝酸溶液浓度偏高的是___(填序号)。
①量取浓硝酸的量筒用蒸馏水洗涤2﹣3次,并把洗涤液转入容量瓶
②容量瓶使用时未干燥
③定容时俯视刻度线
④定容时不小心有少量蒸馏水滴到瓶外
⑤定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu2O广泛应用于太阳能电池领域。以CuSO4、NaOH和抗坏血酸为原料,可制备CuO。
(1)Cu2+基态核外电子排布式为________。
(2)SO42-的空间构型为_______(用文字描述)。
(3)抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为______;推测抗坏血酸在水中的溶解性:_______(填“难溶于水”或“易溶于水”)。
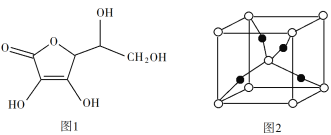
(4)一个Cu2O晶胞(见图2)中,Cu原子的数目为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com