
往含Fe3+、H+、NO3﹣的混合液中加入少量含SO32﹣的某溶液充分反应后(设溶液中的其他成分不反应),下列表示该混合溶液中发生反应的离子方程式中正确的是( )
|
| A. | 2 Fe3++SO32﹣+H2O→2 Fe2++SO42﹣+2 H+ |
|
| B. | 2 H++SO32﹣→SO2↑+H2O |
|
| C. | 2 H++2 NO3﹣+3 SO32﹣→3 SO42﹣+2 NO+H2O |
|
| D. | 2 Fe3++3 SO32﹣+3 H2O→2 Fe(OH)3↓+3 SO2↑ |
| 离子方程式的书写. | |
| 专题: | 离子反应专题. |
| 分析: | 硝酸根离子在酸性环境下氧化性强于三价铁离子的氧化性,二者都能够氧化亚硫酸根离子,往含Fe3+、H+、NO3﹣的混合液中加入少量含SO32﹣的某溶液,亚硫酸根离子先与硝酸根离子反应,依据氧化还原反应规律判断反应产物、配平方程式,据此解答. |
| 解答: | 解:硝酸根离子在酸性环境下氧化性强于三价铁离子的氧化性,二者都能够氧化亚硫酸根离子,往含Fe3+、H+、NO3﹣的混合液中加入少量含SO32﹣的某溶液,亚硫酸根离子先与硝酸根离子反应,反应的离子方程式为:2H++2NO3﹣+3SO32﹣→3SO42﹣+2NO↑+H2O, 故选:C. |
| 点评: | 本题考查了离子方程式的书写,明确氧化还原反应的先后规律是解题关键,注意氧化还原方程式的配平,题目难度中等. |


 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源: 题型:
登山运动员常利用氢化钙固体作为能源提供剂。某兴趣小组用纯净干燥的氢气和金属钙制取氢化钙,所选装置图如下:



A B C D E
图1
查阅资料:①钙易与水反应生成碱和气体。
②氢化钙要密封保存,一旦接触到水就发生反应生成氢氧化钙和氢气。
(1)请按气流方向连接顺序i接( ),( )接( ),( )接( ),k接 a
(填仪器接口的字母编号)。
(2)装置A的作用是 ;装置C的作用是 。
 (3)根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后装入药品;打开分液漏斗活塞, (请按正确的顺序填入下列步骤的序号)。
(3)根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后装入药品;打开分液漏斗活塞, (请按正确的顺序填入下列步骤的序号)。
①加热反应一段时间 ②收集气体并检验其纯度
③关闭分液漏斗活塞 ④停止加热,充分冷却
(4)甲同学设计一个实验,测定上述实验中得到的氢化钙的纯度。请完善下列实验步骤。
①样品称量 ②加入足量的________溶液(填化学式),搅拌、过滤 ③_______、________(填操作名称) ④称量碳酸钙的质量
(5)乙同学利用图2装置测定上述实验中得到的氢化钙的纯度。他称取46 mg 所制得的氢化钙样品,记录开始时注射器活栓停留在10.00 mL刻度处,反应结束后充分冷却,活栓最终停留在57.04 mL刻度处。(上述气体体积均在标准状况下测定)
试通过计算求样品中氢化钙的纯度: 。(计算结果保留一位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期主族元素X、Y、Z、W在元素周期表中的相对位置如下图所示。已知X的最低负价与Y的最高正价代数和为零,下列说法正确的是 ( )
 A.原子半径的大小顺序:r(Y)>r(Z)>r(W)>r(X)
A.原子半径的大小顺序:r(Y)>r(Z)>r(W)>r(X)
B.Z的最高价氧化物的水化物酸性比W的强
C.X的简单气态氢化物的稳定性比W的弱
D.X分别与Y、Z形成的化合物中化学键类型相同
查看答案和解析>>
科目:高中化学 来源: 题型:
若需通过导电实验证明NaCl是离子化合物,可以选择的实验对象是( )
|
| A. | NaCl固体 | B. | NaCl水溶液 | C. | NaCl熔融液 | D. | 以上都不可以 |
查看答案和解析>>
科目:高中化学 来源: 题型:
中的几种,并且水 电离出的c(H+)=1×lO﹣13 mol/L.当向该溶液中缓慢通入一定量的Cl2后,溶液由无色 变为黄色.下列有关分析正确的是( )
|
| A. | 溶液的pH=1或13 | B. | 溶液中一定没有Fe3+,Na+ |
|
| C. | 溶液中阴离子有I﹣,不能确定HCO3﹣ | D. | 当Cl2过量,所得溶液只含有两种盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:
元素周期表中第ⅦA族元素的单质及其化合物的用途广泛.
(1)与氯元素同族的短周期元素的原子结构示意图为 .
(2)能作为氯、溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是 (填序号)
a.Cl2、Br2、I2的熔点
b.Cl2、Br2、I2的氧化性
c.HCl、HBr、HI的热稳定性
d.HCl、HBr、HI的酸性
(3)工业上,通过如下转化可制得KClO3晶体:NaCl溶液 NaClO3溶液
NaClO3溶液 KClO3晶体
KClO3晶体
①完成Ⅰ中反应的总化学方程式: NaCl+ H2O═ NaClO3+ .
②Ⅱ中转化的基本反应类型是 ,该反应过程能析出KClO3晶体而无其他晶体析出的原因是 .
(4)一定条件下,在水溶液中1mol Cl﹣、ClOx﹣(x=1,2,3,4)的能量(kJ)相对大小如图所示.

①D是 ﹣ (填离子符号).
②B→A+C反应的热化学方程式为 (用离子符号表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
下列制取蒸馏水的实验装置与操作的说法中,不正确的是( )
A.蒸馏一定需要温度计
B.冷凝管中的水流方向是从下口进入,上口排出
C.实验中需要在蒸馏瓶中加入几粒碎瓷片,防止出现暴沸现象
D.蒸馏烧瓶必须垫石棉网
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z三种短周期元素,原子半径的大小关系为r(Y)>r(X)>r(Z),原子序数之和为16。X、Y、Z三种元素的常见单质在适当条件下可发生如图所示变化,其中乙和丙均为10电子分子。下列说法不正确的是( ) 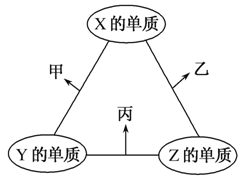
A.元素X位于第ⅥA族
B.甲不能溶解于乙中
C.甲和丙在一定条件下能 发生氧化还原反应
发生氧化还原反应
D.乙的沸点低于丙的沸点
查看答案和解析>>
科目:高中化学 来源: 题型:
在体积恒定的密闭容器中,一定量的SO2与1.100 mol O2在催化剂作用下加热到600 ℃
发生反应:2SO2+O2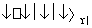 2SO3 ΔH<0。当气体的物质的量减少0.315 mol时反应达到平衡,在相同温度下测得气体压强为反应前的82.5%。下列有关叙述正确的是 ( )
2SO3 ΔH<0。当气体的物质的量减少0.315 mol时反应达到平衡,在相同温度下测得气体压强为反应前的82.5%。下列有关叙述正确的是 ( )
A.当SO3的生成速率与SO2的消耗速率相等时反应达到平衡
B.降低温度,正反应速率减小程度比逆反应速率减小程度大
C.将平衡混合气体通入过量BaCl2溶液中,得到沉淀的质量为161.980 g
D.达到平衡时,S O2的转化率为90%
O2的转化率为90%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com