
有机物DBP常用作纤维素树脂和聚氯乙烯的增塑剂,特别适用于硝酸纤维素涂料。具有优良的溶解性、分散性和粘着性。由有机物A和邻二甲苯为原料可以合成DBP。
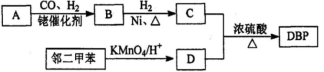
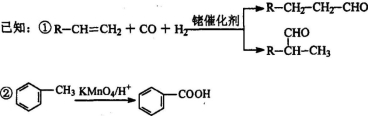
③烃A是有机合成的重要原料。A的质谱图表明其相对分子质量为42,红外光谱表明分子中含有碳碳双键;B能发生银镜反应;有机物C的核磁共振氢谱显示其分子中含有5种化学环境不同的氢原子,且个数之比为3:2:2:2:l。回答下列问题:
(1)A的结构简式为________;A在一定条件下生成聚合物的化学方程式为___________________
(2)D中的含氧官能团是___________。有机物D和足量有机物C反应生成DBP的化学方程式是____________________________________________
(3)下列说法正确的是___________ (选填序号字母)。
A.A能发生聚合反应、加成反应和氧化反应
B.与C互为同分异构体,且含有相同官能团的有机物有2种
C.邻二甲苯能氧化生成D说明有机物分子中基团之间存在影响
D.1 mol DBP可与含4mol NaOH的溶液完全反应
(4)工业上常用有机物E(C8H4O3)代替D生产DBP。反应分为两步进行:
i)E+C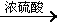 中间产物
中间产物
ii)中间产物+C 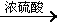 DBP+H2O
DBP+H2O
①请写出E的结构简式___________。
②工业上生产有机物E的反应如下:2X+9O2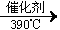 2E+4CO2+4H2O,芳香烃X的一溴代物只有两种,则X的结构简式是___________。
2E+4CO2+4H2O,芳香烃X的一溴代物只有两种,则X的结构简式是___________。
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源:2015-2016学年吉林省高二下学期第一次月考化学试卷(解析版) 题型:选择题
某同学查阅资料时获得对一原子中某电子运动状态的描述,判断其中描述一定错误的是( )
A.能层n=3 能级种类d 自旋状态↑ B.能层n=2 能级种类d 自旋状态↓
C.能层n=4 能级种类p 自旋状态↓ D.能层n=3 能级种类p 自旋状态↑
查看答案和解析>>
科目:高中化学 来源:2016届青海省高三下高考冲刺一理综化学试卷(解析版) 题型:选择题
室温下用下列实验装置进行相应实验,能达到实验目的的是

A.图1:验证浓硫酸具有强氧化性 B.图2:制取干燥的NH3
C.图3:干燥、收集并吸收多余SO2 D.图4:验证乙炔的还原性
查看答案和解析>>
科目:高中化学 来源:2016届宁夏银川一中高三三模理综化学试卷(解析版) 题型:填空题
稀土元素是指元素周期表中原子序数为57到71的15种镧系元素,以及与镧系元素化学性质相似的钪(Sc)和钇(Y)共17种元素。回答下列问题:
(1)钪(Sc)元素的原子核外电子排布式为______________________。镝(Dy)的基态原子电子排布式为[Xe]4f106s2,一个基态镝原子所含的未成对电子数为________。
(2)稀土元素最常见的化合价为+3价,但也有少数还有+4价。请根据下表中的电离能数据判断表中最有可能有+4价的元素是________。几种稀土元素的电离能(单位:kJ·mol-1)
元素 | I1 | I2 | I3 | I4 |
Sc(钪) | 633 | 1 235 | 2 389 | 7 019 |
Y(钇) | 616 | 1 181 | 1 980 | 5 963 |
La(镧) | 538 | 1 067 | 1 850 | 4 819 |
Ce(铈) | 527 | 1 047 | 1 949 | 3 547 |
(3)离子化合物Na3[Sc(OH)6]中,存在的作用力除离子键外还有____________。
(4)Sm(钐)的单质与1,2-二碘乙烷可发生如下反应:
Sm+ICH2CH2I SmI2+CH2=CH2。ICH2CH2I中碳原子杂化类型为______________,1 mol CH2=CH2中含有的σ键数目为________。
SmI2+CH2=CH2。ICH2CH2I中碳原子杂化类型为______________,1 mol CH2=CH2中含有的σ键数目为________。
(5)PrO2(二氧化镨)的晶体结构与CaF2相似,晶胞中镨原子位于面心和顶点。则PrO2(二氧化镨)的晶胞中有________个氧原子。
(6)Ce(铈)单质为面心立方晶体,晶胞参数为a=516 pm,晶胞中Ce(铈)的配位数为________,列式表示Ce(铈)单质的密度:_______g·cm-3(不必计算出结果)。
查看答案和解析>>
科目:高中化学 来源:2016届宁夏银川一中高三三模理综化学试卷(解析版) 题型:选择题
下列关于常见有机化合物的说法中正确的是
A.乙烷和Cl2在光照条件下反应生成6种氯代产物
B.乙醇、乙酸、乙酸乙酯都能发生取代反应,乙酸乙酯中的少量乙酸可用饱和Na2CO3溶液除去
C.乙烯和聚乙烯都能使溴的四氯化碳溶液褪色
D.糖类、油脂和蛋白质都是人体必需的营养物质,它们的组成元素相同
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省高三八模理综化学试卷(解析版) 题型:实验题
中学常采用高锰酸钾加热分解法制取氧气,某兴趣小组经查阅资料获知:制得氧气后固体残余物中的锰酸钾(K2MnO4)具有强氧化性,与还原剂、有机物、易燃物混合可形成爆炸性混合物,如不妥善处置将造成危险。因此该小组对该残余物进行分离提纯,得到锰酸钾晶体,利用回收的锰酸钾与浓盐酸反应制取氯气,并设计实验验证氯气化学性质。
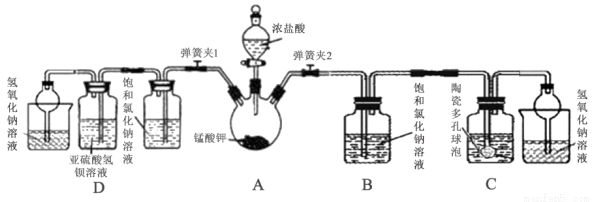
(1)打开分液漏斗活塞及弹簧夹2,观察到烧瓶壁有紫红色物质生成并逐渐消失,黄绿色气体充满烧瓶。反应结束后,烧瓶内有黑色固体残余,写出过程中发生的化学反应方程式:____________。
(2)该方法制取氯气比用纯净的高锰酸钾要缓和平稳许多,试分析原因____________。
(3)该小组利用装置C吸收氯气制备漂白粉。
①C中盛装的试剂为____________;
②陶瓷多孔球泡的作用是____________。
(4)测定漂白粉有效成分的质量分数:称取1.5g所制漂白粉配成溶液,调节pH值并加入指示剂,用0.1000mol/L KI溶液进行滴定,三次平行实验平均每次消耗20.00mL标准液时达到滴定终点,反应原理涉及到的方程式为:3ClO-+I-=3Cl-+ IO3- ; IO3-+5I-+3H2O=6OH-+3I2
①所选的指示剂为____________,达到滴定终点的标志是____________。
②该漂白粉中有效成分的质量分数为____________。
(5)打开分液漏斗活塞及弹簧夹1,可观察到D中的现象为____________ ,该现象能够证明氯气有氧化性。甲同学认为取D中反应后溶液,滴加硝酸酸化的硝酸银,若有白色沉淀产生,也能证明氯气氧化了亚硫酸氢钡,你认为是否正确并说明理由____________。
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省高三八模理综化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.高分子化合物油脂在人体内水解为高级脂肪酸酸和甘油等小分子才能被吸收
B.现代科技已经能够拍到氢键的“照片”,直观地证实了水分子间的氢键是一个水分子中的氢原子与另一个水分子中的氧原子间形成的化学键
C.我国已能利用3D打印技术,以钛合金粉末为原料,通过激光熔化逐层堆积,来制造飞机钛合金结构件,高温时可用金属钠还原相应的氯化物来制取金属钛
D.用活性炭为糖浆脱色和用次氯酸盐漂白纸浆的原理相同
查看答案和解析>>
科目:高中化学 来源:2016届湖北省沙市、沙市五中高考模拟理综化学试卷(解析版) 题型:简答题
氮、磷及其化合物在生产、生活中有重要的用途。回答下列问题:
I (1)直链聚磷酸是由n个磷酸分子通过分子间脱水形成的,常用于制取阻燃剂聚磷酸铵。
①写出磷酸主要的电离方程式________________________。
②直链低聚磷酸铵的化学式可表示为(NH4)(n+2)PnOx,x=_____(用n表示)。
(2)在碱性条件下,次磷酸盐可用于化学镀银,完成其反应的离子方程式。
□H2PO2-+□Ag++□______=□PO43-+□Ag+□______
(3) 工业上生产硝酸铜晶体的流程图如下:
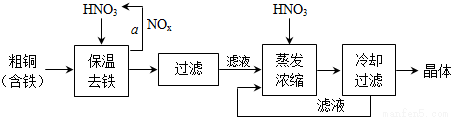
①在步骤a中,需要通入氧气和水,其目的是______.
②进行蒸发浓缩时,要用硝酸调节溶液的pH=1,其目的是(结合离子方程式说明)______.
③下图是某小组同学查阅资料所绘出的硝酸铜晶体[Cu(NO3)2•nH2O]的溶解度曲线(温度在30℃前后对应不同的晶体),下列说法正确的是______(填字母).
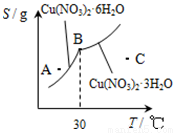
a.A点时的溶液为不饱和溶液
b.B点时两种晶体可以共存
c.按上述流程最终得到的晶体是Cu(NO3)2•3H2O
d.若将C点时的溶液降温至30℃以下,可以析出Cu(NO3)2•6H2O晶体
II (4)查阅资料可知:银氨溶液中存在平衡:Ag+(aq)+2NH3(aq) Ag(NH3)2+(aq),该反应平衡常数的表达式K稳[Ag(NH3)2+]= _________,已知某温度下,K稳[Ag(NH3)2+]=1.10×107,Ksp[AgCl]=1.45×10﹣10。计算得到可逆反应AgCl(s)+2NH3(aq)
Ag(NH3)2+(aq),该反应平衡常数的表达式K稳[Ag(NH3)2+]= _________,已知某温度下,K稳[Ag(NH3)2+]=1.10×107,Ksp[AgCl]=1.45×10﹣10。计算得到可逆反应AgCl(s)+2NH3(aq) Ag(NH3)2+(aq)+Cl-(aq)的化学平衡常数K=_________ (保留2位有效数字),1L 1mol/L氨水中最多可以溶解AgCl_________mol(保留1位有效数字)。
Ag(NH3)2+(aq)+Cl-(aq)的化学平衡常数K=_________ (保留2位有效数字),1L 1mol/L氨水中最多可以溶解AgCl_________mol(保留1位有效数字)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高一下期中化学试卷(解析版) 题型:选择题
元素的性质随着元素原子序数的递增而而呈现周期性变化的原因是( )
A.元素原子的核外电子排布呈周期性变化
B.元素的原子半径呈周期性变化
C.元素的化合价呈周期性变化
D.元素的金属性、非金属性呈周期性变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com