
【题目】氧气、二氧化碳是最常见的气体。回答下列问题:
(1)宇航员呼吸产生的CO2用下列反应处理,实现空间站中的O2循环利用。镍催化剂反应:CO2(g)+4H2(g)![]() CH4(g)+2H2O(g)
CH4(g)+2H2O(g)
①已知H2(g)+![]() O2(g)
O2(g)![]() H2O(g)ΔH=-akJ·mol-1,
H2O(g)ΔH=-akJ·mol-1,
CH4(g)+2O2(g)![]() CO2(g)+2H2O(g)ΔH=-bkJ·mol-1。则镍催化剂反应的ΔH=____kJ·mol-1
CO2(g)+2H2O(g)ΔH=-bkJ·mol-1。则镍催化剂反应的ΔH=____kJ·mol-1
②空间站中所涉及的反应有:
a.镍催化剂反应:CO2(g)+4H2(g)![]() CH4(g)+2H2O(g)
CH4(g)+2H2O(g)
b.电解水反应:2H2O(l)=2H2(g)+O2(g)
c.模拟呼吸反应:C(s)+O2(g)=CO2(g)
则实现空间站O2循环总反应为____
(2)可用O2将HCl转化为Cl2,实现循环利用:O2(g)+4HCl(g)![]() 2Cl2(g)+2H2O(g)。将1molO2和4molHCl充入某恒容密闭容器中,分别在T1和T2的温度下进行实验,测得容器内总压强(p)与反应时间(t)的变化关系如图所示。
2Cl2(g)+2H2O(g)。将1molO2和4molHCl充入某恒容密闭容器中,分别在T1和T2的温度下进行实验,测得容器内总压强(p)与反应时间(t)的变化关系如图所示。

③该反应的速率v=kca(O2)·cb(HCl),k为速率常数),下列说法正确的是____(填标号)。
A.温度升高,k增大
B.使用催化剂,k不变
C.在容器中充入不反应的He,总压增大,k增大
D.平衡后再充入1molO2和4molHCl,k增大
④T1____T2(填“>”或“<”);T1时的转化率____T2时的转化率(填“>”“=”或“<”)。
⑤T1时,HCl的平衡转化率=____;T2反应的Kx=____(Kx为以物质的量分数表示的平衡常数)。
【答案】-4a+b C(s)+2H2(g)=CH4(g) A < > 62.5% ![]()
【解析】
(1)根据盖斯定律进行计算;通过化学反应电解水得到氧气和氢气,氧气为人类呼吸所用,氢气和与人类呼出的二氧化碳反应生成水和甲烷,然后水就又电解生成氧气,这样形成一个循环链,使空间站中的氧气量足够宇航员使用;
(2) ③A.温度改变瞬间,浓度没有影响,即通过增大k从而改变了速率;
B.催化剂降低了反应的活化能,使反应的速率常数k增大;
C.在容器中充入不反应的 He,总压增大分压不变,平衡不变,k 不变;
D.“平衡后再充入1molO2和4molHCl”,相当于增大反应体系的压强;
④根据温度对平衡移动的影响规律,结合图像进行分析;
⑤设反应的O2的物质的量为![]() ,根据反应列出三段式进行分析,根据物质的量之比等于压强之比列方程进行计算;根据平衡常数的计算公式进行计算。
,根据反应列出三段式进行分析,根据物质的量之比等于压强之比列方程进行计算;根据平衡常数的计算公式进行计算。
(1)①设反应H2(g)+![]() O2(g)
O2(g)![]() H2O(g)ΔH=-akJ·mol-1为式①,反应CH4(g)+2O2(g)
H2O(g)ΔH=-akJ·mol-1为式①,反应CH4(g)+2O2(g)![]() CO2(g)+2H2O(g)ΔH=-bkJ·mol-1为式②,反应CO2(g)+4H2(g)
CO2(g)+2H2O(g)ΔH=-bkJ·mol-1为式②,反应CO2(g)+4H2(g)![]() CH4(g)+2H2O(g)可以由②-4×①得出,故该反应的ΔH=-4a+b kJ·mol-1;
CH4(g)+2H2O(g)可以由②-4×①得出,故该反应的ΔH=-4a+b kJ·mol-1;
②由a+b+c得,C(s)+2H2(g)=CH4(g),空间站O2循环总反应为:C(s)+2H2(g)=CH4(g);
(2)③A.刚升温时c(O2)、c(HCl)都不变,升温反应速率增大,故k增大,A正确;
B.催化剂降低了反应的活化能,使反应的速率常数k增大,B错误;
C.充入不反应的He,总压增大,由于是固定容器,原物质的浓度都没变,反应速率不变,故k不变,C错误;
D.平衡后再充入1molO2和4molHCl,c(O2)、c(HCl)都增大,故反应速率增大不一定是由于k增大,D错误;
故选A。
④由图可知,T2先达到平衡,则T1<T2;T2对应的平衡时压强大,则升高温度平衡逆向移动,所以正反应为放热反应,△H<0,因此温度越低,转化率越大,故T1时的转化率大于T2时的转化率;
⑤设反应的O2的物质的量为![]() ,根据题意
,根据题意
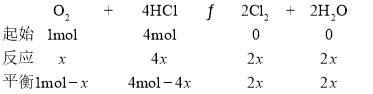
根据物质的量之比等于压强之比,T1有![]() ,解得
,解得![]() mol,故HCl的转化率为
mol,故HCl的转化率为![]() ;T2时,有
;T2时,有![]() ,解得
,解得![]() mol,反应后总物质的量为5-
mol,反应后总物质的量为5-![]() =4.5mol,O2、HCl、Cl2、H2O的物质的量分别为0.5mol、2mol、1mol、1mol,
=4.5mol,O2、HCl、Cl2、H2O的物质的量分别为0.5mol、2mol、1mol、1mol,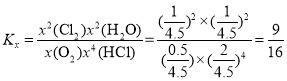


科目:高中化学 来源: 题型:
【题目】由硫铁矿烧渣(主要成分:Fe3O4、Fe2O3和FeO)得到绿矾(FeSO4·7H2O),再通过绿矾制备铁黄[FeO(OH)]的流程如下:烧渣![]()
![]() 溶液
溶液![]() 绿矾
绿矾![]() 铁黄。已知:FeS2和铁黄均难溶于水。下列说法不正确的是( )
铁黄。已知:FeS2和铁黄均难溶于水。下列说法不正确的是( )
A.步骤①,最好用硫酸来溶解烧渣
B.步骤②,涉及的离子反应为FeS2+14Fe3++8H2O═15Fe2++2SO42+16H+
C.步骤③,将溶液加热到有较多固体析出,再用余热将液体蒸干,可得纯净绿矾
D.步骤④,反应条件控制不当会使铁黄中混有Fe(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K、25℃,在NaHS溶液中,各离子的浓度随NaHS溶液浓度的变化关系如图所示,下列叙述不正确的是

已知:298K(25℃)H2S的Ka1=9.10×10-8,Ka2=1.10×10-12。
A.0.10mol/LNaHS溶液:c(Na+)>c(HS)>c(S2)>c(OH)>c(H+)
B.Na2S溶液中:c(Na+)=2c(S2)+2c(HS)+2c(H2S)
C.随着c(NaHS)浓度的增大c(H+)也将持续增大
D.当c(OH)=c(S2)时,c(H+)=10-9mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表为元素周期表中的一部分,表中列出10种元素在周期表中的位置,按要求回答下列各题![]() 请用对应的元素符号作答,填序号无效
请用对应的元素符号作答,填序号无效![]()

(1)化学性质最不活泼的元素符号是______,金属性最强的单质与水反应的化学方程式是______.
(2)①③⑤三种元素最高价氧化物的水化物中碱性最强的物质的化学式是______.
(3)元素①形成的稳定的氧化物在呼吸面具中供氧时的化学方程式是______,该化合物的焰色反应为______色.
(4)②③⑤三种元素形成的离子,离子半径由大到小的顺序是______.
(5)元素⑧的单质和石灰乳作用可制成有漂白和消毒作用的漂白粉,用化学方程式表示漂白粉在潮湿空气中起漂白作用的原理______.
(6)如何证明⑧和⑨元素的非金属性强弱______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家研发出一种新型水溶液锂电池,采用复合膜包裹的金属锂作负极,锰酸锂(LiMn2O4)作正极,以0.5 mol/Li2SO4 水溶液作电解质溶液。电池充、放电时,LiMn2O4与Li2Mn2O4可以相互转化。下列有关该电池的说法正确的是
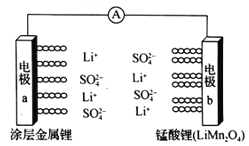
A. 该电池放电时,溶液中的SO42-向电极b移动
B. 该电池负极的电极反应式为:2Li+2H2O==2LiOH+H2↑
C. 电池充电时,外加直流电源的正极与电极a相连
D. 电池充电时,阳极的电极反应式为:Li2Mn2O4-e-==LiMn2O4 +Li+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇既可用于基本有机原料,又可作为燃料用于替代矿物燃料。
(1)以下是工业上合成甲醇的反应:![]()
![]() 下表所列数据是该反应在不同温度下的化学平衡常数
下表所列数据是该反应在不同温度下的化学平衡常数![]() .
.
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
由表中数据判断反应I为 ______ 热反应(填“吸”或“放”) ![]() 某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应,达到平衡后,测得
某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应,达到平衡后,测得![]() ,则CO的转化率为 ______ ,此时的温度为 ______ 从表中选择.
,则CO的转化率为 ______ ,此时的温度为 ______ 从表中选择.
(2)已知在常温常压下:
①![]()
②![]()
③![]()
则反应![]() ______
______ ![]() 用
用![]() 、
、![]() 、
、![]() 表示
表示
(3)处理废水时,最后![]() 以
以![]() 形式除去,当
形式除去,当![]() 时,
时,![]() 沉淀完全,此时溶液的
沉淀完全,此时溶液的![]() ______ (已知,
______ (已知,![]() ,
,![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验不能达到实验目的的是( )
A. 实验室制取氨气
实验室制取氨气
B. 证明乙炔可使溴水褪色
证明乙炔可使溴水褪色
C. 检验蔗糖的水解产物具有还原性
检验蔗糖的水解产物具有还原性
D. 证明溶解度:AgCl>AgI
证明溶解度:AgCl>AgI
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷烯(如图)是由磷原子六元环组成的蜂巢状褶皱二维晶体,它是白磷(![]() )的同素异形体。设NA为阿伏加德罗常数,下列说法正确的是
)的同素异形体。设NA为阿伏加德罗常数,下列说法正确的是
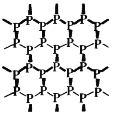
A.3.1g白磷中含P—P键的数目为0.3NA
B.6.2g磷烯中含六元环的数目为0.1NA
C.0.1molP4与0.6molH2在密闭容器中发生反应P4+6H2![]() 4PH3,生成PH3分子的数目为0.4NA
4PH3,生成PH3分子的数目为0.4NA
D.0.1molP4发生反应P4+5O2=2P2O5,转移的电子数为20NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com