
【题目】回答下列问题。
(1)下列物质能导电且属于电解质的是________(填序号)。
A. 固态氯化镁(MgCl2) B. 液态氯化镁(MgCl2)
C. 氯化钠溶液D. 铝
(2)写出下列物质在水溶液中的电离方程式:
①Na2CO3______________;
②H2SO4______________;
③KHSO4_____________。
(3)有人说可将无机化合物KHSO4与NaHCO3归为同一类别,你认为他的理由主要是_____;有人说可将无机化合物KHSO4与H2SO4归为同一类别,你认为他的理由主要是_________________________。
【答案】 B Na2CO3![]() 2Na++CO32- H2SO4
2Na++CO32- H2SO4![]() 2H++SO42- KHSO4
2H++SO42- KHSO4![]() K++H++SO42- KHSO4与NaHCO3都是由金属阳离子和酸式酸根离子构成的无机化合物,都属于酸式盐 KHSO4与H2SO4都能在水溶液中电离出H+,水溶液都显酸性
K++H++SO42- KHSO4与NaHCO3都是由金属阳离子和酸式酸根离子构成的无机化合物,都属于酸式盐 KHSO4与H2SO4都能在水溶液中电离出H+,水溶液都显酸性
【解析】试题分析:本题考查电解质的判断以及物质导电的原因,电离方程式的书写,物质的分类。
(1)A项,固态MgCl2中的阴、阳离子不自由移动,不能导电,MgCl2溶于水和熔融时能导电,固态MgCl2属于电解质;B项,液态MgCl2中阴、阳离子自由移动,能导电,液态MgCl2属于电解质;C项,氯化钠溶液能导电,氯化钠溶液属于混合物,既不是电解质也不是非电解质;D项,铝能导电,铝属于单质,既不是电解质也不是非电解质;答案选B。
(2)①Na2CO3在水溶液中的电离方程式为:Na2CO3=2Na++CO32-。
②H2SO4在水溶液中的电离方程式为:H2SO4=2H++SO42-。
③KHSO4属于强酸的酸式盐,其在水溶液中的电离方程式为:KHSO4=K++H++SO42-。
(3)有人说可将无机化合物KHSO4与NaHCO3归为同一类别,他的理由主要是:KHSO4与NaHCO3都是由金属阳离子和酸式酸根离子构成的无机化合物,都属于酸式盐。有人说可将无机化合物KHSO4与H2SO4归为同一类别,他的理由主要是:KHSO4与H2SO4都能在水溶液中电离出H+,水溶液都显酸性。


科目:高中化学 来源: 题型:
【题目】![]() 是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得
是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得![]() :
:![]()
![]()
![]() ,下列说法中正确的是( )
,下列说法中正确的是( )
A. ![]() 在反应中是还原剂
在反应中是还原剂
B. ![]() 参加反应,在标准状况下能得到22.4L气体
参加反应,在标准状况下能得到22.4L气体
C. 在反应中![]() 既不是氧化剂也不是还原剂
既不是氧化剂也不是还原剂
D. ![]() 参加反应有
参加反应有![]() 电子转移
电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了避免NO、NO2、N2O4对大气的污染,常采用NaOH溶液进行吸收处理(反应方程式:2NO2+2NaOH===NaNO3+NaNO2+H2O;NO2+NO+2NaOH===2NaNO2+H2O)。现有由a mol NO、b mol NO2、c mol N2O4组成的混合气体恰好被V L NaOH溶液吸收(无气体剩余),则此NaOH溶液的物质的量浓度为
A. ![]() mol·L-1 B.
mol·L-1 B. ![]() mol·L-1
mol·L-1
C. ![]() mol·L-1 D.
mol·L-1 D. ![]() mol·L-1
mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某元素R的最高价氧化物的水化物分子式是HnROm,则该元素对应的气态氢化物的化学式为( )
A. H8-n+mR B. H8-2m+nR C. H8-n+2mR D. H8-m+n
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KMnO4常用作氧化剂、防腐剂、消毒剂、漂白剂和水处理剂等。
(1)在K2MnO4溶液中通入CO2可制得高锰酸钾,副产物是黑色沉淀M。该反应中氧化剂与还原剂的质量之比为__________________。由锂离子有机高聚物、锂及M构成原电池,电池反应为Li+M=LiM(s),消耗8.7gM时转移0.1mol电子。则该电池正极的电极反应为___________________________________。
(2)实验室用KMnO4制备O2和Cl2。取0.4mol KMnO4固体加热一段时间后,收集到
amolO2,在反应后的残留固体中加入足量浓盐酸,加热又收集到bmolCl2。设锰元素全部
转化成Mn2+存在于溶液中,当a+b=0.8mol时,在标准状况下生成Cl2的体积为______L;
(3)电解K2MnO4溶液加以制备KMnO4。工业上,通常以软锰矿(主要成分是MnO2)与KOH的混合物在铁坩埚(熔融池)中混合均匀,小火加热至熔融,即可得到绿色的K2MnO4 ,化学方程式为_______________________________。用镍片作阳极(镍不参与反应),铁板为阴极,电解K2MnO4溶液可制备KMnO4。上述过程用流程图表示如下:

则D的化学式为___________;阳极的电极反应式为_____________________;阳离子迁移方向是___________________。
(4)高锰酸钾在酸性介质中还原产物为Mn2+,废液中c(Mn2+)浓度较大时会污染水体。实验室可以用过二硫酸铵[(NH4)2S2O8]溶液检验废水中Mn2+,实验现象是溶液变紫红色(还原产物为SO42-)。过二硫酸可以看成是H2O2的衍生物,过二硫酸铵中含有过氧键(-O-O-)。写出检验Mn2+的离子方程式_________________________________。如果将这个反应设计成盐桥原电池,盐桥中溶液最好选用______________。(选填:饱和KCl溶液、饱和K2SO4溶液或饱和NH4Cl溶液)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】

(I)该硫酸的物质的量浓度是________。
(II)某化学兴趣小组进行硫酸性质的实验探究时,需要240mL1.84mol/L的稀硫酸。可供选抒的仪器由:①玻璃棒 ②烧瓶 ③烧杯 ④胶头滴管 ⑤量筒 ⑥容量瓶 ⑦托盘天平 ⑧药匙 请冋答下列问题:
(1) 上述仪器中,再配置稀硫酸时用不到的有________ (填代号)
(2) 经计算,需:浓硫酸的体积为_____________。现有:
①10mL ②50mL ③100mL三种规格的量筒,你选用的量筒是______ (填代号)
将上述硫酸迸行稀释的实验操作有:___________________。
(3)在配制稀硫酸过程中,其他操作都准确,能引起误差偏高的有:_________ (填代号)
①洗涤量取浓硫酸的量筒,并将洗涤液转移到容量瓶中
②容量瓶用1moll/L稀硫酸润洗
③转移前,容量瓶中含存少量蒸馏水
④量.取浓硫酸时俯视读刻度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用固体NaOH配制0.5 mol/L的NaOH溶液500 mL,①烧杯②100 ml量筒③容量瓶④药匙⑤玻璃棒⑥托盘天平⑦烧瓶
(1)配制时,必须使用的仪器有_____________(填代号),还缺少的仪器是__________________。
(2)在配制的转移过程中某学生进行如图操作,请指出其中的错误:______________、____________。
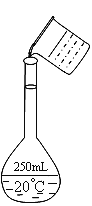
(3)配制时,一般可分为以下几个步骤①称量②计算③溶解④摇匀⑤转移⑥洗涤⑦定容⑧冷却。其正确的操作顺序为_________________。
(4)下列操作会使配制的溶液浓度偏低的是___________(填字母)
A.没有将洗涤液转移到容量瓶 B.转移过程中有少量溶液溅出
C.容量瓶洗净后未干燥 D.定容时俯视刻度线
E.固体NaOH中含有少量Na2O杂质
(5)在容量瓶使用方法中,下列操作不正确的是(填序号) ___________
A.使用容量瓶前检査它是否漏水
B.容量瓶用蒸馏水洗净后,再用碱液润洗
C.将氢氧化钠固体直接放在天平托盘的滤纸上,准确称量并放入烧杯中溶解后,立即注入容量瓶中
D.定容后塞好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转摇匀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知a、b、c三种有机化合物的结构如下:![]() (a)、
(a)、![]() (b)、
(b)、![]() (c)下列有关说法不正确的是( )
(c)下列有关说法不正确的是( )
A. a、b、c的分子式均为C8H8 B. a、b、c中一氯代物最多的为5种
C. a、b、c均能与H2发生加成反应 D. a、b均能使酸性KMnO4溶液褪色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com