
下列关于催化剂的说法正确的是()
A. 催化剂只能加快反应的速率
B. 催化剂在反应中是反应物
C. 催化剂有正催化剂和负催化剂之分
D. 催化剂能使不起反应的物质间发生反应
考点: 催化剂的作用.
专题: 化学平衡专题.
分析: A、负催化剂减慢反应速率;
B、催化剂在反应中是中间产物;
C、催化剂有正催化剂和负催化剂之分;
D、催化剂只能改变化学反应的速率,而不能影响反应的发生与否.
解答: 解:A、负催化剂减慢反应速率,不是一定加快,故A错误;
B、催化剂在反应中是中间产物,故B错误;
C、催化剂有正催化剂和负催化剂之分,正催化剂加快反应速率,负催化剂减慢反应速率,故C正确;
D、催化剂只能改变化学反应的速率,而不能影响反应的发生与否,故D错误;
故选C.
点评: 本题考查催化剂的相关概念,催化剂改变反应速率,而本身在反应前后质量不变,比较容易.


 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案科目:高中化学 来源:2014-2015学年河北省高三下学期期中考试理综化学试卷(解析版) 题型:填空题
(14分)醇是重要的有机化工原料。一定条件下,甲醇可同时发生下面两个反应:
i .2CH3OH(g) CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)
ii.2CH3OH(g) C2H4(g)+2H2O(g)
C2H4(g)+2H2O(g)
I.上述反应过程中能量变化如图所示:
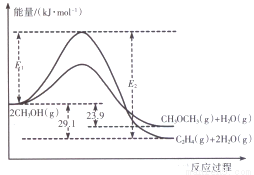
(1)在某密闭容器中,充人一定量CH3OH(g)发生上述两个反应,反应________(填“i”或“ii”)的速率较大,其原因为___________。若在容器中加入催化剂,使ii的反应速率增大,则E1和E2-E1的变化是:E1__________;E2-E1___________(填“增大”、“减小”或“不变”)。
(2)已知:CH3CH2OH(g)=CH3OCH3(g) H=+50.7 kJ·mol-1。则乙烯气相直接水合反应C2H4(g)+H2O(g)=C2H5OH(g)的H= 。
Ⅱ,某研究小组通过控制反应条件,在三个容积均为2 L的密闭容器中只发生反应i,起始反应温度均为T℃,起始投料如下表所示:
起始投料 编号 | CH3OH(g) | CH3OCH3(g) | H2O(g) |
恒温容器1 | 2 | 0 | 0 |
恒温容器2 | 0 | 2 | 2 |
绝热容器3 | 2 | 0 | 0 |
(3)比较平衡时容器1中c1(H2O)和容器2中c2(H2O)的大小:c1(H2O)________c2(H2O)(填 “>”、“<”或“=”);三个容器中反应的化学平衡常数分别记为K1、K2和K3,三者的大小关系为__________。
(4)若容器l中平衡时CH3OH(g) 的转化率为80%,则该温度下反应i的平衡常数K=______________ .
查看答案和解析>>
科目:高中化学 来源: 题型:
将1mol CH4与氯气发生取代反应,待反应完全后,测定生成的四种有机物的物质的量相等,则产生HCl的物质的量是( )
|
| A. | 0.5mol | B. | 2mol | C. | 2.5mol | D. | 4mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
T℃时,在2L的密闭容器中,A气体与B气体发生可逆反应生成C气体,反应过程中A、B、C物质的量变化如图(Ⅰ)所示.若保持其它条件不变,温度分别为T1和T2时,B的物质的量分数与时间关系如图(Ⅱ)所示.下列叙述正确的是( )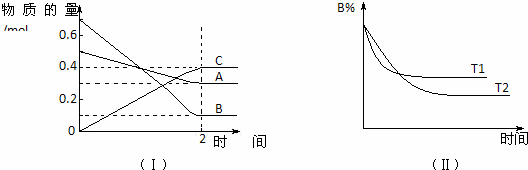
|
| A. | 2 min内A的化学反应速率为0.1 mol/(L•min) |
|
| B. | 在反应达平衡时,保持其他条件不变,增大压强,正逆反应速率都增大,且平衡向逆反应方向移动 |
|
| C. | 在反应达平衡时,其它条件不变,升高温度,正逆反应速率都增大,且A的转化率增大 |
|
| D. | 在T℃时,若A的浓度减少了1 mol/L,则B的浓度会减少3 mol/L,C的浓度会增加2 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:2SO2(g)+O2(g)⇌2SO3(g)△H=﹣196.6kJ•mol﹣1,向密闭容器中加入2mol SO2(g)和1mol O2,一定条件下反应达到平衡,在t2和t4时刻分别只改变一个条件(温度或压强),反应过程中正反应速率如下图所示,下列说法正确的是( )注:t1~t2、t3~t4、t5之后各时间段表示达到平衡状态①、②、③.
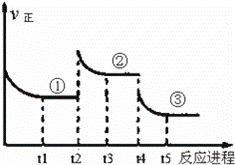
|
| A. | t2~t3时间段,平衡向逆反应方向移动 |
|
| B. | 平衡状态①和②,平衡常数K值相同 |
|
| C. | 平衡状态①和②,SO2转化率相同 |
|
| D. | t4时刻改变的条件是减小压强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
H﹣H、Cl﹣Cl和H﹣Cl的键能分别为436、243和431kJ/mol.请用此数据估计由Cl2、H2反应生成1molHCl时的热效应()
A. 放热183 kJ B. 放热91.5 kJ C. 吸热183 kJ D. 吸热91.5 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
某混合气体可能有CO、CO2、NH3、HCl、H2和水蒸气中的一种或几种,当依次通过澄清石灰水(无浑浊现象)、氢氧化钡溶液(有浑浊现象)、浓硫酸、灼热的氧化铜(变红)和无水硫酸铜(变蓝)时,则可断定该混合气体中一定有( )
A.HCl、CO2、H2 B.CO2、H2、H2O
C.CO、H2、NH3 D.HCl、CO、H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙、丙、丁是中学常见的物质,其中甲、乙、丙均含有同一种元素,在一定条件下的转化关系如图,下列说法正确的是()
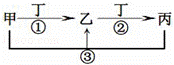
A. 若丁为用量最大,用途最广的金属单质,乙的溶液一定为FeCl3
B. 若通常情况下甲、乙、丙、丁都是气体,且乙和丁为空气的主要成分,则反应①的化学方程式4NH3+5O2 4NO+6H2O
4NO+6H2O
C. 若甲、乙、丙的溶液显碱性,丙可作为医疗上治疗胃酸过多症的药剂,将等物质的量的乙和丙溶于水形成混合溶液,溶液中各离子浓度由大到小的顺序为c(Na+)>c(HCO3﹣)>c(CO32﹣)>c(OH﹣)>c(H+)
D. 若丁为化合物,且为氯碱工业的重要产品,则甲一定为含Al3+的盐
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com