
【题目】下列有关说法错误的是()
A. 在过滤、蒸发、溶解、蒸馏、萃取实验操作中一定要用到玻璃棒的是过滤、蒸发、溶解
B. 200ml 0.25mol/L HCl 溶液与 100ml 0.5mol/L NaCl 溶液所含的 Cl-的物质的量浓度相同
C. 将 5mol/L 的 Mg(NO3)2 溶液 a ml 稀释至 b ml,稀释后溶液中 NO3-的物质的量浓度变为10a/b mol/L
D. 某位同学配制一定物质的量浓度的 NaOH 溶液时,溶解后未冷却至室温就进行后续正常操作, 则造成所配溶液的浓度偏高
【答案】B
【解析】
A、过滤时用玻璃棒引流;蒸发时用玻璃棒搅拌防止局部温度过高使液滴飞溅;溶解固体时用玻璃搅拌是加速溶解的;蒸馏用蒸馏烧瓶,不用玻璃棒;萃取用分液漏斗,不用玻璃棒;选项A正确;B、200ml 0.25mol/L HCl 溶液Cl-的物质的量浓度为0.25mol/L, 100ml 0.5mol/L NaCl 溶液所含的 Cl-的物质的量浓度为0.5mol/L,浓度不相同,选项B错误;C、原溶液中硝酸根离子的物质的量浓度为:c(NO3-)=5mol/L×2=10mol/L,硝酸根离子不发生水解,所以稀释过程中硝酸根离子的物质的量不变,设稀释后溶液中硝酸根离子浓度为c,则:10mol/L×a×10-3L=b×10-3L×c,解得c=![]() mol/L,选项C正确;D、某位同学配制一定物质的量浓度的 NaOH 溶液时,溶解后未冷却至室温就进行后续正常操作, 则造成所配溶液的体积偏小,故溶液浓度偏高,选项D正确。答案选B。
mol/L,选项C正确;D、某位同学配制一定物质的量浓度的 NaOH 溶液时,溶解后未冷却至室温就进行后续正常操作, 则造成所配溶液的体积偏小,故溶液浓度偏高,选项D正确。答案选B。


科目:高中化学 来源: 题型:
【题目】(4分)在有机物:①CH3CH3、②CH2=CH2、③CH3CH2C≡CH、④CH3C≡CCH3、⑤C2H6、⑥CH3CH=CH2中,一定互为同系物的是 ,一定互为同分异构体的是 。(填编号)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以淀粉为主要原料合成一种具有果香味的物质C和化合物D的合成路线如图所示。

(1)A的结构简式为__________,B分子中的官能团名称为__________。
(2)反应⑦中物质X的分子式为__________,反应⑦的反应类型是____________。
(3)反应⑤的化学方程式为________________________________________。反应⑥用于实验室制乙烯,为除去其中可能混有的SO2应选用的试剂是______________________________。
(4)已知D的相对分子量为118,其中碳、氢两元素的质量分数分别为40.68%、5.08%,其余为氧元素,则D的分子式为______________________________。
(5)取少量反应①后的溶液于试管中,证明反应①是否发生,需要的试剂有_____________。
A.NaOH溶液 B.稀硫酸 C.银氨溶液 D.碘水
(6)写出满足以下条件的C的所有同分异构体:能够与NaHCO3反应。________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应实验,能达到实验目的是


①用图 1所示装置从 Fe(OH)3 胶体中过滤出 Fe(OH)3 胶粒
②用图 2所示装置从氯化钠溶液中得到氯化钠晶体
③用图 3所示装置从溴的四氯化碳溶液中分离出四氯化碳
④用图 4所示装置从 C2H5OH 与苯的混合物中分离出苯
⑤用图 5 装置灼烧海带
A. ①②⑤ B. ②③④⑤ C. ②⑤ D. ①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用电导法测定某浓度醋酸电离的ΔH、Ka随温度变化曲线关系如图。已知整个电离过程包括氢键断裂、醋酸分子解离、离子水合。下列有关说法不正确的是
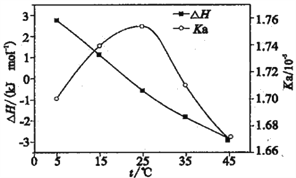
A. 理论上ΔH=0时,Ka最大
B. 25℃时,[CH3COOH]最大
C. 电离的热效应较小是因为分子解离吸收的能量与离子水合放出的能量相当
D. CH3COOH溶液中存在氢键是ΔH随温度升高而减小的主要原因
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】农业生产中用的波尔多液杀菌剂由硫酸铜和石灰乳按一定比例配制而成,它能防治植物病害的原因是( )
A.硫酸铜使菌体蛋白质盐析
B.石灰乳使菌体蛋白质水解
C.菌体蛋白质能溶解于波尔多液中
D.铜离子和石灰乳使菌体蛋白质变性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将50g溶质质量分数为w1,物质的量浓度为c1的浓硫酸沿玻璃棒加入到Vml水中,稀释后得到溶质质量分数为w2,物质的量浓度为c2的稀溶液.下列说法中正确的是( )
A. 若w1=2w2,则c1<2c2,V=50 mL
B. 若w1=2w2,则c1>2c2,V<50 mL
C. 若c1=2c2,则w1<2w2,V<50 mL
D. 若c1=2c2,则w1<2w2,V>50 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)3.01×1023个CO2分子中含______mol氧原子,在标准状况下其体积为______L,它与______gH2O含有相同的氧原子数。
(2)同温同压下,等质量的N2和CO2所含分子数比为______,体积比为______。
(3)某气体在标准状况下的密度为1.25gL-1,则28g该气体所含有的分子数为______。
(4)在标准状况下,22.4L由氮气和氧气组成的混合气体,其质量为30g,则其中氧气的质量为___g。
(5)同温同压下,同体积的H2和A气体的质量分别为1.0g和16.0g,则A的相对分子质量为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com