
| A. | Na+、Fe2+、Cl-、SO42- | B. | K+、Ag+、Cl-、NO3- | ||
| C. | Ba2+、Na+、NO3-、CO32- | D. | Na+、K+、CO32-、SO32- |
 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L庚烷所含有的分子数为NA | |
| B. | 1mol甲基(-CH3)所含电子数为9NA | |
| C. | 标准状况下,CH4和C2H4的混合气体22.4L,所含的分子数为约为NA | |
| D. | 26g C2H2和苯蒸气的混合气体中所含的C原子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 滴加石蕊试液显红色的溶液:Fe3+、NH4+、Cl-、SCN- | |
| B. | pH为1的溶液:Fe2+、K+、ClO-、Cl- | |
| C. | c(H+)=10-12 mol•L-1的溶液:K+、Ba2+、Cl-、NO3- | |
| D. | 存在较多的H+、SO42-、NO3-的溶液:Al3+、CH3COO-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe、Zn | B. | Al、Cu | C. | Al、Fe | D. | Cu、Mg |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ②③④ | C. | ②③ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 其重复结构单元即它的链节是
其重复结构单元即它的链节是 .
.
 CH3COOCH2CH3+H2O.
CH3COOCH2CH3+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
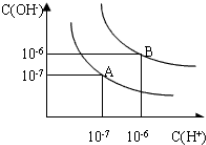
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应中CH3CH2OH表现氧化性 | |
| B. | 该反应发生氧化反应的过程是CrO3→Cr2(SO4)3 | |
| C. | 该反应中氧化产物与还原产物的物质的量之比为2:3 | |
| D. | 该反应中每生成1mol H2O转移1mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 淀粉溶胶中胶体微粒直径大小在1~100nm | |
| B. | 用一束光照射氢氧化铁胶体,可以观察到一条光亮的通路 | |
| C. | 向烧杯中沸腾的蒸馏水里加几滴FeCl3饱和溶液,继续煮沸至液体呈红褐色,停止加热可得氢氧化铁胶体 | |
| D. | 可以利用过滤操作来分离胶体粒子和溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com