
| 15 |
| 16 |

| 1-x+3-3x+2x |
| 1+3 |
| 15 |
| 16 |
| 0.125 |
| 1 |
| ||
| ||



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
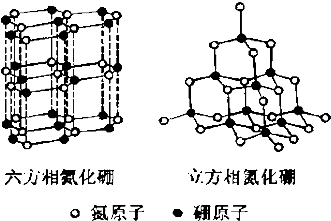 ������BN�������ж�����ṹ�������൪������ͨ�����ڵ��ȶ��࣬��ʯī���ƣ����в�״�ṹ�������������������൪�����dz�Ӳ���ϣ����������ĥ�ԣ����ǵľ���ṹ��ͼ��ʾ��
������BN�������ж�����ṹ�������൪������ͨ�����ڵ��ȶ��࣬��ʯī���ƣ����в�״�ṹ�������������������൪�����dz�Ӳ���ϣ����������ĥ�ԣ����ǵľ���ṹ��ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������½�����������ʵ���Ũ�ȵĴ���������������Һ��ϣ�c��Na+����c��CH3COO-����c��CH3COOH����c��H+����c��OH-�� |
| B����NH4HSO4��Һ�еμӺ������ʵ������ʵ�NaOH��Һ��c��Na+��=c��SO42-����c��NH4+����c��H+����c��OH-�� |
| C����0.1mol/L��NH4��2Fe��SO4��2��Һ�У�c��H+��+c��NH4+��+2c��Fe2+��=c��OH-��+c��SO42-�� |
| D��pH=2�Ĵ�����Һ��pH=12��NaOH��Һ�������ϣ�c��Na+����c��CH3COO-����c��H+����c��OH-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��KMnO4 |
| B��MnO2 |
| C��NaClO3 |
| D��NaClO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ֻ���Ҵ� |
| B��ֻ�������������Ҵ� |
| C��ֻ������ |
| D���Ҵ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Al��OH��3 |
| B��Fe��OH��3 |
| C��CuS |
| D��H2SiO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ͨCO��һ���ǵ�ص����� |
| B�������缫��Ӧ�ǣ�O2+2CO2+4e-=2CO32- |
| C����������CO32-�����ʵ����ڹ���ʱ���ֲ��� |
| D����������������Ӧ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com