
| 化学键 | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C |
| 键能/kJ?mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
| ||
. |
| A、+236 kJ?mol-1 |
| B、-236 kJ?mol-1 |
| C、+412 kJ?mol-1 |
| D、-412 kJ?mol-1 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
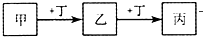 甲、乙、丙、丁均为中学化学常见的物质,它们之间的转化关系如图(反应条件及其它产物已略去).下列说法不正确的是( )
甲、乙、丙、丁均为中学化学常见的物质,它们之间的转化关系如图(反应条件及其它产物已略去).下列说法不正确的是( )| A、若甲是AlCl3溶液,则丁可能是NaOH溶液 |
| B、若甲是Cl2,则丁可能是Fe |
| C、若丁是CO2,则甲可能为Mg |
| D、若丁是HCl,则甲一定是Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4Cl=NH3↑+HCl↑ |
| B、NaCl+AgNO3=AgCl↓+NaNO3 |
| C、CaO+CO2=CaCO3 |
| D、Mg+2HCl=MgCl2+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、原子半径:W>Z>Y>X>M |
| B、XZ2、X2M2、W2Z2均为直线形的共价化合物 |
| C、CaX2、CaM2和CaZ2等3种化合物中,阳离子与阴离子个数比为1:2 |
| D、由X、Y、Z、M四种元素共同形成的化合物中一定有共价键可能有离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等于2a% | B、大于2a% |
| C、小于2a% | D、无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将58.5g NaCl固体溶于1 L水中所得溶液 |
| B、将22.4L HCl气体溶于水配成1 L的溶液 |
| C、从1L 10mol/L的浓盐酸中取出的100mL溶液 |
| D、将4g NaOH固体溶于水中配成的100 mL溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Zn+2 HCl═ZnCl2+H2↑ | ||||
| B、2 H2S+SO2═3S↓+2 H2O | ||||
C、H2+CuO
| ||||
D、2 H2O
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在通常条件下,1mol氩气含有的原子数为2NA |
| B、56g金属铁由原子变为离子时失去的电子数为NA |
| C、在标准状况下,2.24 L氨气所含的电子总数约为NA |
| D、1 mol/L 的 Na2SO4溶液中含有Na+个数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 纯净物 | 混合物 | 强电解质 | 弱电解质 | 非电解质 | |
| A | 盐酸 | 水煤气 | 硫酸 | 醋酸 | HD |
| B | 胆矾 | 石灰水 | 硫酸钡 | Al(OH)3 | NH3 |
| C | 火碱 | 蔗糖溶液 | 氯化钠 | 氨水 | 三氧化硫 |
| D | 冰醋酸 | 福尔马林 | 苛性钾 | 碘化氢 | 乙醇 |
| A、A | B、B | C、C | D、.D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com