
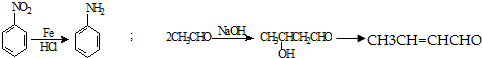
| ��Ӧ�Լ� |
| ��Ӧ���� |
| ��Ӧ�Լ� |
| ��Ӧ���� |
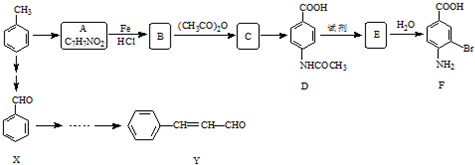
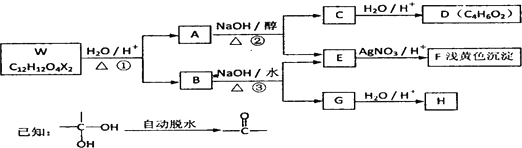
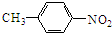 ��A������Ϣ�з�Ӧ����������ԭΪ��������B����B�Ľṹ��ʽΪ
��A������Ϣ�з�Ӧ����������ԭΪ��������B����B�Ľṹ��ʽΪ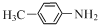 �����D�Ľṹ��֪��B�а�����1��Hԭ�ӱ�ȡ������CΪ
�����D�Ľṹ��֪��B�а�����1��Hԭ�ӱ�ȡ������CΪ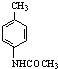 ��C�����Ը��������Һ��������D���Ա�D��F�Ľṹ��֪��D��Һ�巢��ȡ����Ӧ����EΪ
��C�����Ը��������Һ��������D���Ա�D��F�Ľṹ��֪��D��Һ�巢��ȡ����Ӧ����EΪ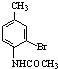 ��E����ˮ�ⷴӦ�õ�F����֪B��C��Ϊ�˱������������������ױ��������ڹ��������·�����ȡ����Ӧ�õ�
��E����ˮ�ⷴӦ�õ�F����֪B��C��Ϊ�˱������������������ױ��������ڹ��������·�����ȡ����Ӧ�õ� ������ˮ�ⷴӦ����
������ˮ�ⷴӦ����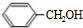 ���ٷ�������������
���ٷ�������������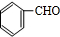 ������Ϣ��֪������ȩ����ȩ�ڼ��������µõ�
������Ϣ��֪������ȩ����ȩ�ڼ��������µõ�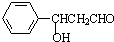 ���ٷ�����ȥ��Ӧ�õ�
���ٷ�����ȥ��Ӧ�õ�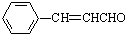 ���ݴ˽��н��
���ݴ˽��н�� ��A������Ϣ�з�Ӧ����������ԭΪ��������B����B�Ľṹ��ʽΪ
��A������Ϣ�з�Ӧ����������ԭΪ��������B����B�Ľṹ��ʽΪ �����D�Ľṹ��֪��B�а�����1��Hԭ�ӱ�ȡ������CΪ
�����D�Ľṹ��֪��B�а�����1��Hԭ�ӱ�ȡ������CΪ ��C�����Ը��������Һ��������D���Ա�D��F�Ľṹ��֪��D��Һ�巢��ȡ����Ӧ����EΪ
��C�����Ը��������Һ��������D���Ա�D��F�Ľṹ��֪��D��Һ�巢��ȡ����Ӧ����EΪ ��E����ˮ�ⷴӦ�õ�F����֪B��C��Ϊ�˱�����������������
��E����ˮ�ⷴӦ�õ�F����֪B��C��Ϊ�˱����������������� +��CH3CO��2O��
+��CH3CO��2O��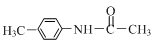 +CH3COOH��
+CH3COOH�� +��CH3CO��2O��
+��CH3CO��2O�� +CH3COOH��
+CH3COOH�� ����ͬ���칹�壺�ٱ�����ֻ�����ֲ�ͬ��ѧ��������ԭ�ӣ��ڷ����к���ȩ���������������л���Ľṹ��ʽ��
����ͬ���칹�壺�ٱ�����ֻ�����ֲ�ͬ��ѧ��������ԭ�ӣ��ڷ����к���ȩ���������������л���Ľṹ��ʽ��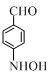 ��
��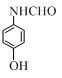 ��
��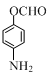 ��
�� ����
����  ��
�� ����
���� ���ٷ�����ȥ��Ӧ�õ�
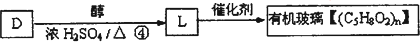
���ٷ�����ȥ��Ӧ�õ�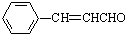 ��������ϩ��ˮ�����ӳɷ�Ӧ�����Ҵ����Ҵ������������õ���ȩ�����Ա���ȩ����ϩΪԭ�Ϻϳ�Y��·������ͼΪH2C=CH2
��������ϩ��ˮ�����ӳɷ�Ӧ�����Ҵ����Ҵ������������õ���ȩ�����Ա���ȩ����ϩΪԭ�Ϻϳ�Y��·������ͼΪH2C=CH2| H2O |
| ���� |
| O2 |
| Cu���� |
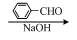

| Ũ���� |
| �� |
 ��
��| H2O |
| ���� |
| O2 |
| Cu���� |


| Ũ���� |
| �� |
 ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Ħ���DZ�ʾ���ʵ����ĵ�λ |
| B��������������Һ�����ǽ���ķ�ɢ������ֱ����1 nm��100nm֮�� |
| C��������ԭ��Ӧ��ʵ���ǵ��ӵĵ�ʧ����Ӷ�ƫ�� |
| D��ÿ������ɫ��Ӧʵ���Ҫ��Na2CO3��Һ����ϴ��˿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
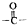 c��-CHO
c��-CHO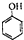 ��
��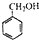 ���õ��Լ���
���õ��Լ���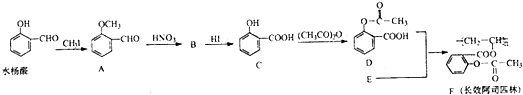
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʳ�� | ����֭ | �����ݲ� | ţ�� | ������ |
| ����pH��Χ | 3.0��4.0 | 3.2��3.6 | 6.3��6.6 | 7.6��8.0 |
| A���������Լ��� |
| B��θ��������Ӧ�ٳԳ����ݲ� |
| C������֭��ʹʯ����Һ��� |
| D��ţ�̱ȼ�����ļ���ǿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| t/s | 0 | 5 | 15 | 25 | 35 |
| n��A��/mol | 1.0 | 0.85 | 0.81 | 0.80 | 0.80 |
| A����Ӧ��ǰ5 s��ƽ������v��A��=0.17 mol?L-1?s-1 |
| B�����������������䣬�����¶ȣ�ƽ��ʱc��A��=0.41 mol?L-1����Ӧ�ġ�H��0 |
| C����ͬ�¶��£���ʼʱ�������г���2.0 mol C���ﵽƽ��ʱ��C��ת���ʴ���80% |
| D����ͬ�¶��£���ʼʱ�������г���0.20 mol A��0.20 mol B��1.0 mol C����Ӧ�ﵽƽ��ǰv��������v���棩 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
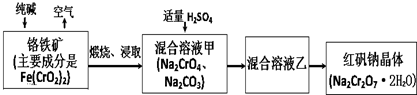
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Mg��Al |
| B��Mg��Cu |
| C��Cu��Zn |
| D��Al��Fe |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
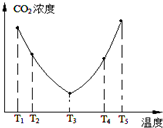 ��Ⱦ�뻷�������Ѿ���Ϊ�����ҹ������ŵ�һ�����⣬��Ⱦ��Ϊ������Ⱦ��ˮ��Ⱦ��������Ⱦ�ȣ�
��Ⱦ�뻷�������Ѿ���Ϊ�����ҹ������ŵ�һ�����⣬��Ⱦ��Ϊ������Ⱦ��ˮ��Ⱦ��������Ⱦ�ȣ�| 1 |
| 2 |
| 1 |
| 2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com