
| A. | CuO、Na2O和Na2O2都是碱性氧化物 | |
| B. | SO2能与碱反应生成盐和水,因此SO2属于酸性氧化物 | |
| C. | NH4Cl不含金属阳离子,不属于盐 | |
| D. | 金属氧化物都是碱性氧化物 |
分析 A.和酸反应生成盐和水的氧化物为碱性氧化物,反应为复分解反应;
B.和碱反应生成盐和水的氧化物为酸性氧化物,反应为复分解反应;
C.金属阳离子和酸根阴离子构成的化合物为盐;
D.金属氧化物可以是碱性氧化物、酸性氧化物、两性氧化物.
解答 解:A.CuO、Na2O都是碱性氧化物,Na2O2和酸反应生成的盐、水和氧气,不是碱性氧化物,故A错误;
B.SO2能与碱反应生成盐和水,符合酸性氧化物的概念,因此SO2属于酸性氧化物,故B正确;
C.NH4Cl不含金属阳离子,但是含铵根离子、氯离子,属于盐,故C错误;
D.金属氧化物可以是碱性氧化物如Na2O、也可以是酸性氧化物Mn2O7、也可以是两性氧化物如Al2O3,故D错误;
故选B.
点评 本题考查了物质分类、物质组成、物质性质等知识点,概念实质理解是解题关键,题目难度不大.


 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA | |
| B. | 0.5molO3与11.2LO2所含的分子数一定相等 | |
| C. | 物质的量浓度为0.5mol/L MgCl2溶液,含有Cl-数为NA | |
| D. | 1molFe与足量稀盐酸反应时,转移电子的数目为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 用一张已除去表面氧化膜的铝箔紧紧包裹在试管外壁(如图),将试管浸入硝酸汞溶液中,片刻取出,然后置于空气中,不久铝箔表面生出“白毛”,红墨水柱右端上升.根据实验现象判断下列说法错误的是( )
用一张已除去表面氧化膜的铝箔紧紧包裹在试管外壁(如图),将试管浸入硝酸汞溶液中,片刻取出,然后置于空气中,不久铝箔表面生出“白毛”,红墨水柱右端上升.根据实验现象判断下列说法错误的是( )| A. | 实验中发生的反应都是化合反应 | B. | 铝是一种较活泼的金属 | ||
| C. | 铝与氧气反应放出大量的热量 | D. | 铝片上生成的白毛是氧化铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验法 | B. | 分类法 | C. | 观察法 | D. | 比较法 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 56g金属铁完全反应时失去的电子数为一定为2NA | |
| B. | 18g水所含的电子数目为NA | |
| C. | 在常温常压下,48g氧气和臭氧的混合气体所含的原子数目为3NA | |
| D. | 在常温常压下,11.2L二氧化硫所含的分子数目为0.5 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝热反应是炼铁最常用的方法 | |
| B. | 硅是现代光学及光纤制品的基本原料 | |
| C. | 采用“静电除尘”“燃煤固硫”“汽车尾气催化净化”等方法可提高空气质量 | |
| D. | 袋装食品常用生石灰包作为食品的抗氧化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “水乳交融,火上浇油”前者包含物理变化,后者包含化学变化 | |
| B. | “滴水石穿.绳锯木断”不包含化学变化 | |
| C. | “蜡炬成灰泪始干”包含的是物理变化 | |
| D. | 石灰吟中“烈火焚烧若等闲”指的是加热,不包含化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
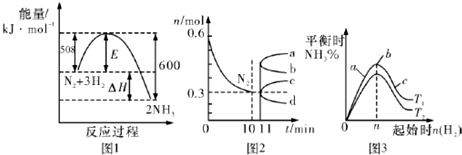
| A. | 升高温度,该反应的平衡常数增大 | |
| B. | 由图2信息,10 min内该反应的平均速率v(H2)=0.09 mol•L-1•min-1 | |
| C. | 由图2信息,从11 min起其它条件不变,压缩容器的体积,则n(N2)的变化曲线为d | |
| D. | 图3中温度T1<T2,a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是b点 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com