
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2015-2016学年山东省滕州市高一上学期12月月考化学试卷(解析版) 题型:选择题
向下列溶液中通入过量的CO2,有沉淀产生的是
A.澄清的石灰水 B.饱和碳酸钠溶液 C.氯化钙溶液 D.硝酸钡溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高二上学情调查化学试卷(解析版) 题型:选择题
下列反应的离子方程式正确的是
A.FeBr2溶液中通入过量Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-
B.硫酸亚铁溶液中加过氧化氢溶液:Fe2++2H2O2+4H+=Fe3++4H2O
C.用氨水吸收少量二氧化硫:NH3·H2O+SO2=NH4++HSO3-
D.硝酸铁溶液中加过量氨水:Fe3++3NH3·H2O=Fe(OH)3↓+3NH4+
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三上学期期末理综化学试卷(解析版) 题型:实验题
【化学──选修2:化学与技术】
以黄铁矿(主要成分是FeS2)为原料生产硫酸的工艺流程图如下:
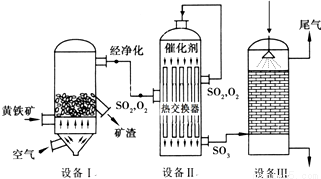
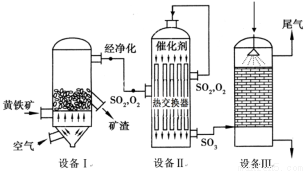 (1)依据工艺流程图判断下列说法不正确的是(选填序号字母)___________。
(1)依据工艺流程图判断下列说法不正确的是(选填序号字母)___________。
A.为使黄铁矿充分燃烧,需将其粉碎
B.过量空气能提高SO2的转化率
C.排出的矿渣可供炼铁
D.使用催化剂能提高SO2的化学反应速率和转化率
E.设备I生成的气体经净化的主要目的是防止催化剂中毒
F.热交换器的目的是使SO2的热量传递给SO3,有利于SO2的氧化和SO3的吸收
(2)设备Ⅰ的名称为 ,燃烧黄铁矿的化学方程式为 。
(3)设备Ⅱ为接触室,采用常压而不采用高压的原因是 。在生产中,为提高催化剂效率采取的措施有 。
(4)设备Ⅲ为吸收塔,从顶部喷淋 吸收SO3,得到 ,不用水吸收SO3是为了 。吸收塔中填充有许多瓷管,其作用是 。
(5)吸收塔排出的尾气先用氨水吸收,再用浓硫酸处理,得到较高浓度的SO2和铵盐。SO2既可作为原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的Br2。SO2吸收Br2的离子方程式是 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上学期12月月考化学试卷(解析版) 题型:填空题
利用核磁共振技术测定有机物分子的三维结构的研究获得了2002年诺贝尔化学奖。在有机物分子中,不同氢原子的核磁共振谱中给出的峰值(信号)也不同,根据峰值(信号)可以确定有机物分子中氢原子的种类和数目。例如二乙醚的结构简式为:CH3—CH2—O—CH2—CH3,其核磁共振谱中给出的峰值(信号)有两个,如图所示:
(1) 下列物质中,其核磁共振氢谱中给出的峰值(信号)只有一个的是 。
A.CH3CH3 B.CH3COOH
C.CH3COOCH3 D.CH3OCH3
(2) 化合物A和B的分子式都是C2H4Br2, A的核磁共振氢谱图如右图所示,则A的结构简式为: ,请预测B的核磁共振氢谱上有 个峰(信号)。
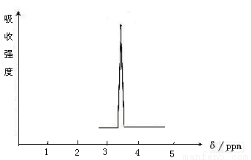
(3)用核磁共振氢谱的方法来研究C2H6O的结构,简要说明根据核磁共振氢谱的结果来确定C2H6O分子结构的方法是 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上12月月考化学试卷(解析版) 题型:选择题
在铁制品上镀一定厚度的锌层,以下方案设计正确的是
A.锌作阳极,镀件作阴极,溶液中含有锌离子
B.铂作阴极,镀件作阳极,溶液中含有锌离子
C.铁作阳极,镀件作阴极,溶液中含有亚铁离子
D.锌作阴极,镀件作阳极,溶液中含有锌离子
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省邯郸市高二上学期第三次月考化学试卷(解析版) 题型:选择题
下列各组烃的混合物,只要总质量一定,按任意比例混合,完全燃烧后生成的CO2和H2O都是恒量的是( )
A.C2H2、C2H4 B.C2H4、C4H6 C.C2H6、C3H6 D.C6H6、C2H2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西钦州港经济开发区中学高二上12月月考化学试卷(解析版) 题型:计算题
将 4 g NaOH溶于多少克水中,才能使每100个水分子中溶有一个Na +
查看答案和解析>>
科目:高中化学 来源:2016届福建省闽粤联合体高三上学期第三次联考化学试卷(解析版) 题型:推断题
已知甲、乙、丙、X是4种中学化学中常见的物质,其转化关系符合下图(反应条件省略)

(1)若甲为气态非金属单质,丙能与人体血液中的血红蛋白结合而使人中毒,则乙的电子式为 。
(2)若甲为黄绿色气体,X为常见的金属,则X在元素周期表中的位置是 ,丙的水溶液呈 (填酸性、碱性或中性),原因是: (用离子方程式表示)。含amol乙的溶液溶解了一定量X后,若溶液中两种金属阳离子的物质的量恰好相等,则被还原的乙的物质的量是 mol。
(3)若X为酸性氧化物且具有漂白性,甲溶液的焰色反应呈黄色,则标准状况下8.96 L 气体X与2 L 0.25 mol/L的甲溶液反应生成的溶液中乙和丙的物质的量浓度之比为(不考虑离子的水解) 。另有和丙具有相同元素组成的物质丁,丙和丁能反应生成气体,写出该反应的离子方程式 。
(4)若X为强碱溶液,乙为白色胶状沉淀,则甲与丙反应的离子方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com