
| 变化过程 | △H | △S |
| 4Fe(s)+3O2(g)=2Fe2O3(s) | <0 | |
| CaCO3(s)分解为CaO(s)和CO2(g) |
| 时间/min | A | B | C | D |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | 0.100 | 0.200 | 0.100 | 0.100 |
| 4 | 0.100 | 0.200 | 0.100 | 0.100 |
| 5 | 0.116 | 0.216 | 0.084 |
分析 (1)Fe在氧气中燃烧是放热反应;碳酸钙的分解反应是吸热反应,该反应中有气体生成,熵增大;
(2)①反应3min时各物质的浓度不变,反应达到平衡状态,该反应的正反应是放热反应,升高温度平衡逆向移动,平衡常数减小,先计算该温度下的平衡常数,根据平衡常数确定温度;
②反应在4min~5min之间,A和B浓度增大而C浓度减小,说明平衡逆向移动,改变的条件应该是增大D浓度.
解答 解:(1)Fe在氧气中燃烧是放热反应,所以△H<0;碳酸钙分解是吸热反应,所以△H>0,该反应中有气体生成,所以△S>0,
故答案为:<0;>0;>0
(2)①反应3min时各物质的浓度不变,反应达到平衡状态,该温度下的化学平衡常数K=$\frac{0.100×0.100}{0.100×0.200}$=0.5<1,该反应的正反应是放热反应,升高温度平衡逆向移动,化学平衡常数减小,所以该温度大于850℃,
故答案为:大于;
②反应在4min~5min之间,A和B浓度增大而C浓度减小,说明平衡逆向移动,即向左移动,且C减小的浓度与A或B增加的浓度等,所以改变的条件应该是增大D浓度,
故答案为:向左;C.
点评 本题考查化学平衡计算及焓变和熵变,为高频考点,侧重考查学生分析判断及计算能力,化学平衡常数只与温度有关,对于吸热反应来说升高温度化学平衡常数增大,对于放热反应来说升高温度化学平衡常数减小,题目难度不大.


科目:高中化学 来源: 题型:解答题
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AgCl的溶解度增大 | B. | AgCl的溶解度、溶度积KSP均不变 | ||
| C. | AgCl的溶度积KSP增大 | D. | AgCl的溶解度、溶度积KSP均增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质的溶解性为难溶,则该物质的溶解度为0 | |
| B. | 某离子被沉淀完全是指该离子在溶液中的浓度为0 | |
| C. | 通过沉淀反应能将大部分杂质离子沉淀 | |
| D. | 难溶电解质的溶度积越小,溶解度越大 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
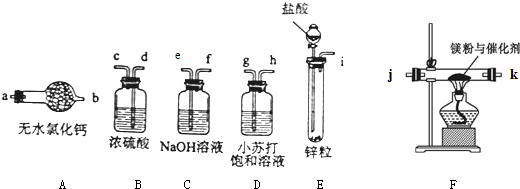
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com