
| A. | 明矾做净水剂:Al3++3H2O═Al (OH)3↓+3H+ | |
| B. | 小苏打治疗胃酸过多:CO32-+2H+═CO2↑+H2O | |
| C. | 漂白液加白醋,提高漂白效率:CH3COOH+ClO-═HClO+CH3COO- | |
| D. | 酸化的淀粉碘化钾溶液在空气中放置一段时间变蓝:4I-+O2+2H2O═2I2+4OH- |
分析 A.铝离子水解生成的是氢氧化铝胶体,不能使用沉淀符号;
B.小苏打为碳酸氢钠,碳酸氢根离子不能拆开;
C.醋酸的酸性大于次氯酸,二者能够反应才次氯酸;
D.酸性条件下,反应产物中不会生成氢氧根离子.
解答 解:A.明矾做净水剂的正确离子方程式为:Al3++3H2O?Al(OH)3(胶体)+3H+,故A错误;
B.小苏打治疗胃酸过多,碳酸氢根离子不能拆开,正确的离子方程式为:HCO3-+H+═CO2↑+H2O,故B错误;
C.漂白液加白醋,能够发生反应:CH3COOH+ClO-═HClO+CH3COO-,提高了漂白效率,故C正确;
D.酸化的淀粉碘化钾溶液在空气中放置一段时间变蓝,碘离子被氧化成碘单质,正确的离子方程式为:4I-+O2+4H+═2I2+2H2O,故D错误;
故选C.
点评 本题考查了离子方程式的书写判断,题目难度中等,注意明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.


 优等生题库系列答案
优等生题库系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 下列框图所示的物质转化关系中,甲是日常生活中常见的金属,乙、丙、丁是常见的气体单质.气体B与气体C相遇产生白烟,A是强碱,D的焰色反应呈紫
下列框图所示的物质转化关系中,甲是日常生活中常见的金属,乙、丙、丁是常见的气体单质.气体B与气体C相遇产生白烟,A是强碱,D的焰色反应呈紫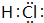 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子中的C、H、O的个数比为1:2:1 | B. | 分子中C、H个数比为1:2 | ||
| C. | 该有机物的相对分子质量为14 | D. | 该分子中肯定不含氧元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 根据以上信息,可推断NH3•H2O为弱电解质 | |
| B. | 加水稀释过程中,c(H+)•c(OH-) 的值增大 | |
| C. | 加入K2CO3固体可促进 NH4+的水解 | |
| D. | 同pH的NH4Cl溶液和CH3COOH溶液,由水电离出的c(H+) 前者大 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 实验操作 | 实验目的 | |
| A | 向甲酸钠溶液中加新制的Cu(OH)2并加热 | 确定甲酸钠具有醛基性质 |
| B | 苯中有少量苯酚,加入氢氧化钠溶液后,分液 | 除去苯中混有的苯酚 |
| C | 向酒精和水的混合溶液中加入金属钠 | 确定酒精中混有水 |
| D | 将氯乙烷与氢氧化钠溶液共热一段时间,再向冷却后的混合液中滴加硝酸银溶液 | 检验水解产物中的氯离子 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 12.3 | B. | 11.7 | C. | 11.3 | D. | 12.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将SO2通入酸性KMnO4 溶液中,紫色褪去 证明SO2具有漂白性 | |
| B. | 在滴有酚酞的Na2CO3溶液中,加入CaCl2溶液后红色褪去 证明Na2CO3溶液中存在水解平衡 | |
| C. | 向1mL0.2mol/L NaOH溶液中滴入2滴0.1mol/L的MgCl2溶液产生白色沉淀后,再滴加2滴0.1mol/L的FeCl3溶液,又生成红褐色沉淀 证明在相同温度下,氢氧化镁的溶解度大于氢氧化铁的溶解度 | |
| D. | 测定等物质的量浓度的HCl与H2S溶液的pH,后者较大 证明非金属性Cl>S |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com