
| A. | ③④⑤ | B. | ②③⑤ | C. | ①③④⑤ | D. | ②③④⑤ |
分析 ①SO2能与Ba(OH)2溶液反应:SO2+Ba(OH)2=BaSO3↓+H2O,BaSO3+SO2+H2O=Ba(HSO3)2;
②盐酸酸性大于亚硫酸,二氧化硫与氯化钙不反应;
③二氧化硫与硫化氢反应生成单质硫,硫不溶液水,有沉淀;
④二氧化硫通入硝酸钡,二氧化硫被氧化生成硫酸根离子,硫酸根离子与钡离子反应生成硫酸钡沉淀;
⑤酸性亚硫酸大于硅酸,则反应生成硅酸沉淀.
解答 解:①SO2能与Ba(OH)2溶液反应:SO2+Ba(OH)2=BaSO3↓+H2O,BaSO3+SO2+H2O=Ba(HSO3)2,所以足量的二氧化硫无沉淀生成,故不选;
②盐酸酸性大于亚硫酸,二氧化硫与氯化钙不反应,无浑浊,故不选;
③二氧化硫与硫化氢反应生成单质硫,硫不溶液水,有沉淀,故选;
④二氧化硫通入硝酸钡,二氧化硫被氧化生成硫酸根离子,硫酸根离子与钡离子反应生成硫酸钡沉淀,故选;
⑤酸性亚硫酸大于硅酸,则反应生成硅酸沉淀,故选;
故选A.
点评 本题考查二氧化硫的化学性质,为高频考点,把握二氧化硫的还原性及发生的氧化还原反应为解答的关键,题目难度不大.


 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 加成→消去→取代 | B. | 消去→加成→水解 | C. | 取代→消去→加成 | D. | 消去→加成→消去 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
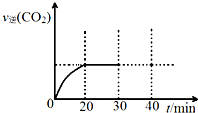 消除大气污染有多种方法.
消除大气污染有多种方法.| 浓度/mol•L-1 时间/min | NO | N2 | CO2 |
| 0 | 1.00 | 0 | 0 |
| 10 | 0.58 | 0.21 | 0.21 |
| 20 | 0.40 | 0.30 | 0.30 |
| 30 | 0.40 | 0.30 | 0.30 |
| 40 | 0.32 | 0.34 | 0.17 |
| 50 | 0.32 | 0.34 | 0.17 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 镁离子的电子式:Mg2+ | B. | HF的电子式:H:F | ||
| C. | Cl-离子的结构示意图: | D. | NH4Cl的电子式: |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
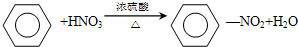 ,属于取代反应;
,属于取代反应; ,属于加成反应;
,属于加成反应; +Br2$\stackrel{FeBr_{3}}{→}$
+Br2$\stackrel{FeBr_{3}}{→}$ +HBr,属于取代反应;
+HBr,属于取代反应;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验事实 | 理论解释 |
| A | 足球烯(C60)在苯中的溶解度比在乙醇中的溶解度大 | C60易溶于非极性溶剂苯而难溶于乙醇,符合相似相溶原理 |
| B | Fe3+可用SCN-检验 | 生成了Fe(SCN)3红色沉淀 |
| C | Cu(OH)2可溶于氨水 | 可生成深蓝色溶液[Cu(H2O)4]SO4 |
| D | HF的沸点高于HCl | HF的键长比HCl短 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO | B. | Fe2O3 | C. | CO2 | D. | Fe |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 项目 | 实验目的 | 实验方案 |
| A | 验证稀硫酸和稀硝酸的氧化性强弱 | 将两块相同的铜片分别加入浓度均为2mol/L的硫酸和硝酸中,观察反应的难易程度 |
| B | 验证Cu、Fe的还原性强弱 | 将铁丝和铜丝分别插入浓硝酸中,观察反应的剧烈程度 |
| C | 验证Br、I非金属性强弱 | 将少量溴水加入KI-淀粉溶液中,观察溶液是否变蓝色 |
| D | 验证Mg、Al的金属性强弱 | 在Mg(OH)2、Al(OH)3中分别加入稀氨水,观察沉淀能否溶解 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com