
| A. | 补血剂中铁元素的化合价为+2价 | |
| B. | 铝是人体中的一种微量元素,如果摄入量过多,易患老年痴呆症 | |
| C. | 铝能溶解于氢氧化钠溶液中,而铁不能与氢氧化钠溶液反应 | |
| D. | 铝的导热性比铁强,因而用铝锅煮食物比铁锅好 |
分析 A、亚铁血红蛋白输送氧气,缺铁导致营养性贫血;
B、人体内铝元素摄入量过多易患老年痴呆症;
C、铝能和氢氧化钠溶液反应,而铁不能;
D、根据铁锅中含有人体所需的铁元素进行解答.
解答 解:A、亚铁血红蛋白输送氧气,缺铁导致营养性贫血,补血剂中含有+2价铁元素,故A正确;
B.人体内铝元素摄入量过多易患老年痴呆症,故B正确;
C、铝能和氢氧化钠溶液反应,而铁不能,故C正确;
D、研究证实,长期使用铝制品作炊具可使铝摄入过量,对健康不利,还可导致老年性痴呆的发生率增加,所以,炒菜还是用铁锅好,而使用铁锅一定程度上能防止缺铁性贫血,故D错误.
故选D.
点评 本题考查Al与Fe的性质、人体营养平衡等,难度不大,注意对基础知识的掌握.


 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案科目:高中化学 来源: 题型:实验题
 水杨酸甲酯对多种细菌的繁殖和黏附有抑制作用,也是安全、有效的植物生长调节剂.实验室制备水杨酸甲酯装置示意图和有关数据如下:
水杨酸甲酯对多种细菌的繁殖和黏附有抑制作用,也是安全、有效的植物生长调节剂.实验室制备水杨酸甲酯装置示意图和有关数据如下:| 相对分子 质量 | 沸点/℃: | 在水中的溶解性 | |
| 甲醇 | 32 | 64.7 | 与水以任何比例相溶 |
| 水杨酸 | 138 | 211 | 0.22g/100ml |
| 水杨酸甲酯 | 152 | 222 | 0.07g/100ml |
 +CH3OH$\stackrel{H+}{?}$
+CH3OH$\stackrel{H+}{?}$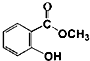 +H2O
+H2O查看答案和解析>>
科目:高中化学 来源: 题型:解答题
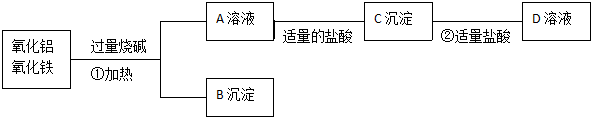
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | ||
| Z | W |
| A. | W 的最高价氧化物的水化物酸性比Z的强 | |
| B. | 原子半径:Z>W,离子半径:Z<W | |
| C. | Y的气态氢化物可与W的气态氢化物反应生成一种离子化合物 | |
| D. | X元素形成的化合物种类最多 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
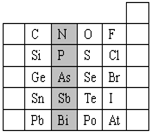 元素在周期表中的位置,反映了元素的原子结构和元素的性质.如图是元素周期表的一部分.
元素在周期表中的位置,反映了元素的原子结构和元素的性质.如图是元素周期表的一部分.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg2+、Na+、Cl-、SO42- | B. | K+、Na+、Cl-、AlO2- | ||
| C. | Cu2+、Ca2+、Br-、I- | D. | Ba2+、K+、Cl-、HCO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com