
| A. | 含有共价键的化合物一定是共价化合物 | |
| B. | 非金属元素之间可以形成离子化合物 | |
| C. | 不同元素的原子构成的分子只含极性共价键 | |
| D. | 主族元素的最外层电子数一定等于其最高化合价 |
分析 A.离子化合物一定含有离子键,可能含有共价键;
B.铵盐属于离子化合物;
C.不同元素的原子构成的分子可能含有非极性键;
D.O、F没有最高正价.
解答 解:A.共价化合物只含有共价键,离子化合物一定含有离子键,可能含有共价键,则含有共价键的化合物不一定是共价化合物,如NaOH属于离子化合物含有共价键,故A错误;
B.非金属元素之间可以形成离子化合物,如铵盐属于离子化合物,由非金属元素构成,故B正确;
C.不同元素的原子构成的分子中一定含极性共价键,可能含有非极性共价键,如H2O2,故C错误;
D.D.O、F没有最高正价,其它的主族元素的最外层电子数一定等于其最高化合价,故D错误.
故选B.
点评 本题考查共价键与离子键、离子化合物与共价化合物的区别,题目难度不大,注意相关基础知识的积累.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 甲烷和氯气的混合气体在光照后,瓶壁上有油状液滴附着 | |
| B. | 苯在一定温度、压强和催化剂的作用下和氢气反应,生成环己烷 | |
| C. | 乙烯通入酸性高锰酸钾溶液中,高锰酸钾溶液褪色 | |
| D. | 将灼热的铜丝迅速插入乙醇中,反复多次,有刺激性气味产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn与浓H2SO4反应产生22.4LSO2,则反应中转移电子数目为2NA | |
| B. | 1 mol Na2O和Na2O2固体中含有的阴、阳离子总数为3NA | |
| C. | 3.4 g H2O2中含有的共用电子对数为0.1NA | |
| D. | 1 mol•L-1的氯化铵溶液中含有NH${\;}_{4}^{+}$的数目小于NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高氯酸铵为离子化合物 | |
| B. | 高氯酸铵中只含有离子键 | |
| C. | 高氯酸铵中既有离子键又有共价键,同时还有配位键 | |
| D. | 高氯酸铵中阴、阳离子的个数比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| X | 原子M层上的电子数是原子核外电子层数的2倍 |
| Y | 短周期中原子半径最大的元素 |
| Z | 元素的单质为双原子分子,Z的氢化物水溶液呈碱性 |
| W | 元素最高正价是+7价 |
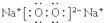 .用电子式表示元素X与Y形成化合物的过程
.用电子式表示元素X与Y形成化合物的过程 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解氯化镁制备镁,电解氯化铝也能制备铝 | |
| B. | ⅣA族元素氢化物沸点顺序是:GeH4>SiH4>CH4;则ⅤA族元素氢化物沸点顺序也是:AsH3>PH3>NH3 | |
| C. | 第二周期元素氢化物的稳定性顺序是:HF>H2O>NH3;则第三周期元素氢化物的稳定性顺序也是:HCl>H2S>PH3 | |
| D. | 干冰(CO2)是分子晶体,则SiO2也是分子晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
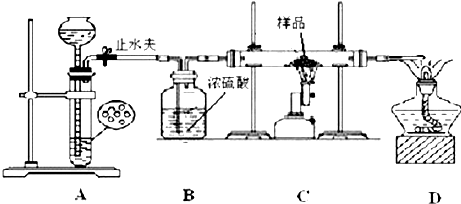
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
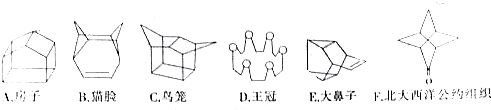
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com