
 �Ķ��������в��ϣ�
�Ķ��������в��ϣ�| ���� | �۵�/�� | �е�/�� | �ܶ�/g•cm-3 | �ܽ��� |
| �Ҷ��� C2H6O2 | -11.5 | 198 | 1.11 | ������ˮ���Ҵ��������л��ܼ� |
| ������ C3H8O3 | 17.9 | 290 | 1.26 | �ܸ�ˮ�;ƾ�������Ȼ��ܣ������������л��ܼ� |
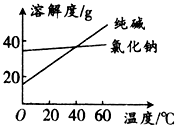
���� ��1���ܽ�����߱仯��֪̼�����ܽ�����¶��������仯���Ȼ����ܽ�����¶ȱ仯����������Ȼ��ƺʹ���Ļ�����з���������������ܽ�Ȳ��죬�Ʊ�������Һ����ȴ�ᾧ�ķ�������̼���ƾ��壻���Ҷ����ͱ��������Һ���������ͼ�������зе㲻ͬ��������������ķ��������¶ȷ������
��2������̼�����е��Ȼ��ƣ����������ӵļ��鷽�����ʵ�鲽����飻
��3����ȡmg������Ʒ��������������ᣬ��ַ�Ӧ�����������ա����ص�bg���壬�������ɵ��Ȼ�����������Ʒ������ʽ���㣬���з����ķ�ӦΪ̼���ƺ����ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼��
��ȡmg������Ʒ������ˮ����������Ȼ�����Һ�����ˡ�ϴ�ӡ���ɡ����ص�ag���壬Ϊ̼��Ƴ��������������̼Ԫ���غ���㣻
��� �⣺��1���ܽ�����߱仯��֪̼�����ܽ�����¶��������仯���Ȼ����ܽ�����¶ȱ仯����������Ȼ��ƺʹ���Ļ�����з���������������ܽ�Ȳ��죬��������Ȼ��ƺʹ���Ļ�����з�����������ʵķ����ǣ��ܽ⡢����Ũ������ȴ�ᾧ�����ˣ����Ҷ����ͱ��������Һ����룬����ͼ�������зе㲻ͬ��������������ķ��������¶ȷ������
�ʴ�Ϊ��C������
��2��ij������Ʒ�п��ܺ����Ȼ��ƣ����ʵ��֤���IJ�������������ͽ���Ϊ��ȡ��Ʒ�������Թ��У���������ˮ�ܽ⣬���������ữ����������Һ�����ְ�ɫ������֤�������Ȼ��ƣ�
�ʴ�Ϊ��ȡ��Ʒ�������Թ��У���������ˮ�ܽ⣬���������ữ����������Һ�����ְ�ɫ������֤�������Ȼ��ƣ�
��3���ٷ���1�漰�ķ�Ӧ�Ļ�ѧ����ʽΪ��Na2CO3+2HCl=2NaCl+H2O+CO2�����ʴ�Ϊ��Na2CO3+2HCl=2NaCl+H2O+CO2����
��ȡmg������Ʒ������ˮ����������Ȼ�����Һ�����ˡ�ϴ�ӡ���ɡ����ص�ag���壬Ϊ̼��Ƴ��������������̼Ԫ���غ����õ�̼���Ƶ���������=$\frac{\frac{ag}{100g/mol}��106g/mol}{mg}$��100%=$\frac{53a}{50m}$��100%��
�ʴ�Ϊ��$\frac{53a}{50m}$��100%��
���� ���⿼�������ʷ��뷽�������ʺ����ⶨ���������ʵķ���Ӧ�ã����ջ����ǽ���ؼ�����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������ʳ�üӵ��Σ���KIO3���к��е� | |
| B�� | �ôס�����ʯ��ˮ��֤�����к���̼���� | |
| C�� | �õ�Ƽ����������Ƿ��в������� | |
| D�� | �ü����ס�ʳ�Ρ�ˮ��ɵ����ʵ��ܽ⡢����ʵ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��ѧʽ | ����ƽ�ⳣ����25�棩 |
| HCN | K=4.9��10-10 |
| CH3COOH | K=1.8��10-5 |
| H2CO3 | K1=4.3��10-7��K2=5.6��10-11 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ںϳɰ���ҵ�У���ѹ���������NH3�IJ��� | |
| B�� | ֱ��ȼ��ú���罫ú������ӹ�����ȼ�յ�Ч�ʺ� | |
| C�� | ��ʯȼ�ϰ���ʯ�͡���Ȼ����ú������ | |
| D�� | ��ʱ������������£��ӽ����Ϸ��������У�������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
 ��Bԭ�ӵĺ�������Ų�ʽ1s22s22p63s23p2��Cԭ�ӵļ۵����Ų�ʽ3s23p5��
��Bԭ�ӵĺ�������Ų�ʽ1s22s22p63s23p2��Cԭ�ӵļ۵����Ų�ʽ3s23p5���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | �٢ڢ� | B�� | �ܢݢ� | C�� | �ڢܢ� | D�� | �ۢܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ˮʱ��ƽ�����淴Ӧ�����ƶ� | |
| B�� | ��������CH3COONa���壬ƽ�����淴Ӧ�����ƶ���c��CH3COO-������ | |
| C�� | ��������0.1 mol•L-1HCl��Һ��ƽ�����淴Ӧ�����ƶ�����Һ��c��H+����С | |
| D�� | ��������NaOH���壬ƽ��������Ӧ�����ƶ���������ǿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
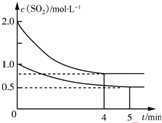 ��ס��������ݻ���Ϊ1L�ĺ��º��ݵ��ܱ������У��ֱ����һ������SO2��O2�����У��׳���2mol SO2��1mol O2���ҳ���1mol SO2��0.5mol O2����������Ӧ��2SO2��g��+O2��g��?2SO3��g����H=-197.74kJ•mol-1��һ��ʱ���ﵽƽ�⣬�����������c��SO2����mol•L-1����ʱ��t��min���ı仯��ϵ��ͼ��ʾ������˵����ȷ���ǣ�������
��ס��������ݻ���Ϊ1L�ĺ��º��ݵ��ܱ������У��ֱ����һ������SO2��O2�����У��׳���2mol SO2��1mol O2���ҳ���1mol SO2��0.5mol O2����������Ӧ��2SO2��g��+O2��g��?2SO3��g����H=-197.74kJ•mol-1��һ��ʱ���ﵽƽ�⣬�����������c��SO2����mol•L-1����ʱ��t��min���ı仯��ϵ��ͼ��ʾ������˵����ȷ���ǣ�������| A�� | �ų�������Q��Q���ף���2Q���ң� | |
| B�� | ��ϵ��ѹǿp��p���ף���2p���ң� | |
| C�� | ����ǰ5 min�ڵķ�Ӧ����v��O2��=0.05mol•L-1•min-1 | |
| D�� | ���������������䣬����ʼʱ�����г���0.4 mol SO2��0.2 mol O2��0.4 mol SO3�����ʱv��������v���棩 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com