
| A.工业上用氧气在接触室中氧化黄铁矿得到二氧化硫 |
| B.工业上通过电解饱和氯化钠溶液制备金属钠 |
| C.工业用氨氧化法制硝酸是人工固氮过程 |
| D.生产普通玻璃的主要原料有石灰石、石英和纯碱 |
 口算能手系列答案
口算能手系列答案科目:高中化学 来源:不详 题型:实验题
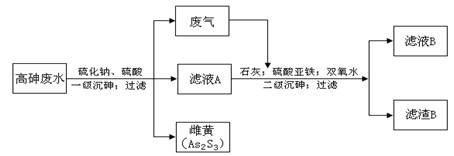
 类型)被吸收。
类型)被吸收。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
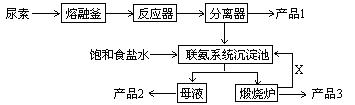
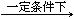 C3N6H6 + 6NH3 + 3CO2
C3N6H6 + 6NH3 + 3CO2查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
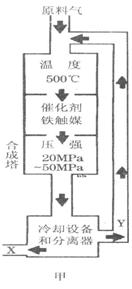
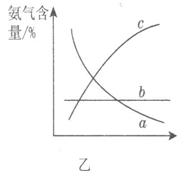
 ②图甲中条件选定的主要原因是(选填字母序号,下同)________。
②图甲中条件选定的主要原因是(选填字母序号,下同)________。 某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
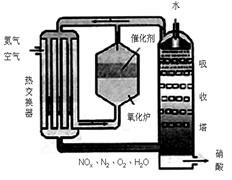
 4NO(g)+6H2O(l) △H<0
4NO(g)+6H2O(l) △H<0 2NO2(g) △H<0
2NO2(g) △H<0 2HNO3(l) +NO(g) △H<0
2HNO3(l) +NO(g) △H<0| A.适当升高温度 | B.适当增大吸收塔内的压强 |
| C.增大空气中O2的浓度 | D.吸收塔内填充瓷环,增大气液接触面 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
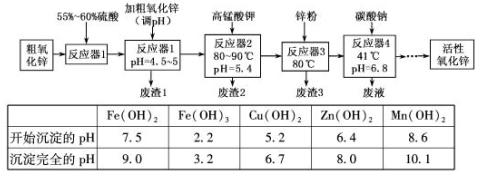
 -1
-1 重,得到ZnO 2.43g和标准状况下CO20.224l,碱式碳酸锌的化学式
重,得到ZnO 2.43g和标准状况下CO20.224l,碱式碳酸锌的化学式查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
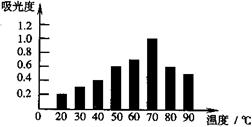
| A.20℃时,红枣中红色素含量最低 | |
| B.吸光度越大,红枣中红色素含量越高 | C.红色素可能在较高温度下不稳定 |
| D.温度越高,提取液中红色素含量越高 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com