
| A.H2S2O7 | B.H2S3O10 | C.H4S3O12 | D.H2S4O13 |
科目:高中化学 来源:不详 题型:填空题
| | 熔点/℃ | 沸点/℃ | 密度/g·cm—3 | 水 |
| CS2 | —110.8 | 46.5 | 1.26 | 难溶 |
| S2Cl2 | —76 | 138 | 1.75 | 水解 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NaN3中含有离子键 |
| B.1 mol NaN3完全分解最多可以产生33.6L N2 |
| C.当有4.2g N2生成时,转移电子数约为6.02×1022 |
| D.常温下,NaN3化学性质稳定,包装盒上无需特别说明注意事项 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
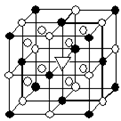
| | 熔点/K | 沸点/K | 标准状况时在水中的溶解度 |
| H2S | 187 | 202 | 2.6 |
| H2O2 | 272 | 423 | 以任意比互溶 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

| A.极性共价键; | B.非极性共价键; | C.配位键; | D.离子键;E.金属键;F.σ键;G.π键 |
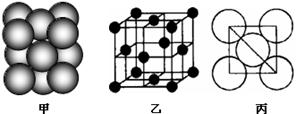
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.分子间作用力 | B.氢键 | C.非极性共价键 | D.极性共价键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.四个共价键的键长完全相同 |
| B.四个共价键的键长完全不同 |
| C.原来的三个N-H的键长完全相同,但与由配位键形成的N-H键不同。 |
| D.四个N-H键键长相同,但键能不同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com