
分析 (1)根据向沸水中逐滴滴加饱和FeCl3溶液生成氢氧化铁胶体,根据胶体分析;
(2)铜与氯化铁反应生成氯化铁、氯化亚铁;检验溶液中Fe3+存在通常用KSCN溶液,溶液变红说明Fe3+存在;
(3)氧化还原反应中,化合价升高元素在反应中被氧化,化合价降低元素在反应中被还原,得到还原产物,化合价降低值=化合价升高值=转移电子数,据此回答;
解答 解:(1)向沸水中逐滴滴加饱和FeCl3溶液,至液体呈透明的红褐色,生成氢氧化铁胶体,胶体的微粒直径的范围是1~100nm,故答案为:1~100;
(2)铜与氯化铁反应生成氯化铁、氯化亚铁,反应方程式为:2FeCl3+Cu═2 FeCl2+CuCl2,检验溶液中Fe3+存在通常用KSCN溶液,取少量溶液与试管中,滴加KSCN溶液,溶液变红说明Fe3+存在,该反应的离子方程式为Fe3++SCN-=[Fe(SCN)]2+,
故答案为:2FeCl3+Cu═2 FeCl2+CuCl2;KSCN溶液;
(3)反应2Fe(OH)3+3NaClO+4NaOH═2Na2FeO4+3NaCl+5H2O中,Fe元素化合价升高,氢氧化铁是还原剂,根据化合价规则,Na2FeO4中Fe是+6价,在反应中Na2FeO4是氧化产物,该反应中,化合价降低值=化合价升高值=转移电子数=6,所以每生成1mol Na2FeO4反应中转移电子的物质的量为3mol,
故答案为:Fe(OH)3;3NA;
点评 本题考查了铁离子的检验与性质、胶体的微粒大小、氧化还原反应中电子的转移和氧化还原反应中的基本概念知识等,属于基础知识的考查,题目难度不大,注意基础知识的记忆掌握.


科目:高中化学 来源: 题型:实验题
 如图是某学校实验室从化学试剂商店买回的硫酸试剂瓶标签上的部分内容.现用该浓硫酸配制500mL浓度为1mol•L-1的稀硫酸.可供选用的仪器有:
如图是某学校实验室从化学试剂商店买回的硫酸试剂瓶标签上的部分内容.现用该浓硫酸配制500mL浓度为1mol•L-1的稀硫酸.可供选用的仪器有:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2H++2e-═H2↑ | B. | 2H2O+O2+4e-═4OH- | ||
| C. | Fe-2e-═Fe2+ | D. | 4OH--4e-═O2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
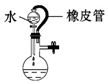 | 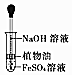 | 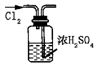 |  |
| A.证明该装置气密性良好 | B.观察Fe(OH)2的生成 | C.干燥Cl2 | D.比较Na2CO3与NaHCO3的稳定性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4.6 gNa与O2完全反应,生成7g产物时失去电子的物质的量为0.2 mol | |
| B. | Na与稀硫酸反应的离子方程式为2Na+2H+=2Na++H2↑ | |
| C. | 将少量Na投入到CuSO4溶液中,既有沉淀生成又有气体放出 | |
| D. | 金属钠着火可以用泡沫灭火器或用干燥的沙土灭火 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去NaCl溶液中少量CaCl2:加入适量Na2CO3,过滤 | |
| B. | 用四氯化碳可以从碘水中萃取碘 | |
| C. | Na2CO3固体中含有少量NaHCO3杂质可用加热的方法提纯 | |
| D. | 既可用品红溶液或酸性KMnO4溶液鉴别 CO2和SO2,也可用澄清石灰水鉴别 CO2和SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向FeCl2溶液中通入Cl2:Fe2++Cl2═Fe3++2Cl- | |
| B. | Ba(OH)2溶液与硫酸反应:OH-+H+═H2O | |
| C. | 次氯酸钙溶液中通入少量SO2:2ClO-+Ca2++SO2+H2O═CaSO3↓+2HClO | |
| D. | 碳酸氢钠溶液中加入过量石灰水:HCO3-+Ca2++OH-═CaCO3↓+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com